
(8分)2013年以来全国各地都遭遇“十面霾伏”。其中,二氧化硫、氮氧化物和可吸入颗粒物是雾霾的主要组成成分。综合治理其污染是环境化学当前的重要研究内容。
(1)NO2有较强的氧化性,能将SO2氧化生成SO3,本身被还原为NO,已知下列两反应过程中能量变化如图所示:
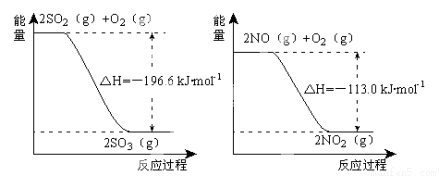
则NO2氧化SO2的热化学方程式为 _____________________________ 。
(2)SO2与O2反应时的平衡转化率与温度、压强的关系如图所示。根据图示回答下列问题:

①压强:Pl P2(填“>”、“=”或“<”)。
②平衡常数:A点 B点(填“>”、“=”或“<”)。
③200℃下,将一定量的SO2和O2充人体积为1 L的密闭容器中,经10min后测得容器中各物质的物质的量如下表所示:
气体 | SO2 | O2 | SO3 |
物质的量(mol) | 1.6 | 1.8 | 0.4 |
10min内该反应的反应速率v(O2)= ;该反应达到化学平衡状态的标志是 。
a.SO2和O2的体积比保持不变 b.体系的压强保持不变
c.混合气体的密度保持不变 d.SO2和SO3物质的量之和保持不变
(3)用NH3催化还原NOx可以消除氮氧化物的污染。
①写出氨气消除NO污染的化学方程式 ___________________________ ;
②若还原产物比氧化产物多0.5mol,则反应转移电子数为 ________ 。
(1)NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=-41.8kJ/mol(1分)
SO3(g)+NO(g) ΔH=-41.8kJ/mol(1分)
(2)①<(1分)②=(1分)③0.02mol/(L·min) (1分) ab(1分)
(3)①4NH3+6NO=5N2+6H2O(2分) ②6mol或6×6.02×1023(1分)
【解析】
试题分析:(1)根据图像1可得:①2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ?mol?1,根据图像2可得:②2NO(g)+O2(g)=2NO2(g) ΔH=-113.0kJ?mol?1,根据盖斯定律:①×1/2—②×1/2得NO2(g)+SO2(g)
2SO3(g) ΔH=-196.6kJ?mol?1,根据图像2可得:②2NO(g)+O2(g)=2NO2(g) ΔH=-113.0kJ?mol?1,根据盖斯定律:①×1/2—②×1/2得NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=-41.8kJ?mol?1;(2)①SO2与O2反应的反应为气体物质的量减小的反应,增大压强,平衡正向移动,二氧化硫的转化率增大;由图像可知,压强为P2时二氧化硫平衡转化率较大,即压强:Pl <P2;②由图像可知,A、B两点温度相同,平衡常数的影响因素为温度,故平衡常数:A点=B点;③根据公式v=△n/V△t 代入题给数据计算v (SO3)=0.4mol/1L×10min=0.04mol/(L·min),根据速率之比等于化学计量数之比得10min内该反应的反应速率v(O2)= 0.02mol/(L·min);根据“变量不变,已达平衡”判断;a.分析题给数据知,随着反应的进行SO2和O2的体积比不断变化,当其保持不变时已达平衡,正确;b.随着反应的进行容器内气体的物质的量不断减小,体系的压强不断减小,当其保持不变时已达平衡,正确;c.等容条件下混合气体的密度为恒量,不能作平衡标志,错误;d.SO2和SO3物质的量之和始终为2mol,不能作平衡标志,错误,选ab。(3)①氨气与NO反应生成氮气和水,利用化合价升降法配平,化学方程式为4NH3+6NO=5N2+6H2O;②根据上述反应知,该反应转移的电子数为12e-,还原产物比氧化产物多1mol,若还原产物比氧化产物多0.5mol,则反应转移电子数为6mol或6×6.02×1023。
SO3(g)+NO(g) ΔH=-41.8kJ?mol?1;(2)①SO2与O2反应的反应为气体物质的量减小的反应,增大压强,平衡正向移动,二氧化硫的转化率增大;由图像可知,压强为P2时二氧化硫平衡转化率较大,即压强:Pl <P2;②由图像可知,A、B两点温度相同,平衡常数的影响因素为温度,故平衡常数:A点=B点;③根据公式v=△n/V△t 代入题给数据计算v (SO3)=0.4mol/1L×10min=0.04mol/(L·min),根据速率之比等于化学计量数之比得10min内该反应的反应速率v(O2)= 0.02mol/(L·min);根据“变量不变,已达平衡”判断;a.分析题给数据知,随着反应的进行SO2和O2的体积比不断变化,当其保持不变时已达平衡,正确;b.随着反应的进行容器内气体的物质的量不断减小,体系的压强不断减小,当其保持不变时已达平衡,正确;c.等容条件下混合气体的密度为恒量,不能作平衡标志,错误;d.SO2和SO3物质的量之和始终为2mol,不能作平衡标志,错误,选ab。(3)①氨气与NO反应生成氮气和水,利用化合价升降法配平,化学方程式为4NH3+6NO=5N2+6H2O;②根据上述反应知,该反应转移的电子数为12e-,还原产物比氧化产物多1mol,若还原产物比氧化产物多0.5mol,则反应转移电子数为6mol或6×6.02×1023。
考点:考查热化学方程式的书写、盖斯定律,化学反应速率和化学平衡,氧化还原方程式的书写和计算。


科目:高中化学 来源:2015届江苏省高三上学期期中考试化学试卷(解析版) 题型:选择题
25oC时,2amol·L-1氢氟酸水溶液中,用NaOH溶液调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如下图所示。下列说法正确的是
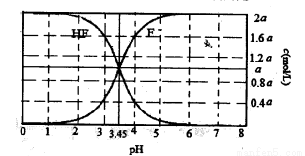
A.当c(F一)>c(HF)时,溶液呈碱性
B.当pH=3时,溶液中c(F一)<c(Na+)
C.当pH=3.45时,所加NaOH溶液恰好与HF完全反应
D.当pH=4时,溶液中:c(HF)+c(Na+)+c(H+)-c(OH-)=2amol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江苏省中学高三上学期第一次月考化学试卷(解析版) 题型:选择题
一定条件下存在反应:2SO2(g)+O2(g) 2SO3(g),△H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g),△H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是

A.容器I、Ⅲ中平衡常数相同
B.容器II、Ⅲ中正反应速率相同
C.SO3的体积分数:Ⅱ>III
D.容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源:2015届广东省高三9月月考化学试卷(解析版) 题型:简答题
(16分)脱羧反应形成新的C-C键为有机合成提供了一条新的途径,例如:

(1)化合物I的分子式为_________,化合物I含有的官能团名称是______________,
1mol化合物I完全燃烧需要消耗_____mol O2。
(2)化合物III与新制氢氧化铜反应的化学方程式为________________________。
(3) 与
与 也可以发生类似反应①的反应,有机产物的结构简式为:_________________________。
也可以发生类似反应①的反应,有机产物的结构简式为:_________________________。
(4)化合物I有多种同分异构体,请写出任意2种符合下列条件的同分异构体的结构简式:
___________。(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
查看答案和解析>>
科目:高中化学 来源:2015届广东省高三9月月考化学试卷(解析版) 题型:选择题
下列化学用语或模型表示正确的是( )
A.Cl-离子的结构示意图: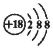 B.CCl4分子的球棍模型:
B.CCl4分子的球棍模型:
C.乙烯的结构简式 CH2CH2 D.H2O2的结构式:H—O—O—H
查看答案和解析>>
科目:高中化学 来源:2015届江西南昌三中高三11月份月考化学试卷(解析版) 题型:选择题
CuSO4是一种重要的化工原料,其有关制备途径及性质如下图所示。下列说法不正确的是
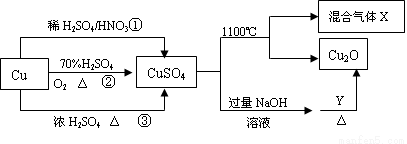
A.相对于途径①、③,途径②更好地体现了绿色化学思想
B.若Y是有机物,则Y只可属醛类
C.1molCuSO4在1100℃所得混合气体X用足量硝酸钡溶液吸收可得沉淀233g
D.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
查看答案和解析>>
科目:高中化学 来源:2015届江西南昌三中高三11月份月考化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z原子序数之和为28,X+与Z2-具有相同的核外电子层结构,Y、Z在同一周期。下列推测正确的是
A.元素Y的最高化合价为+7
B.三种元素的原子半径rZ>rY>rX
C.Z的单质比Y的单质更易与H2反应
D.化合物X2Z2中阴阳离子数之比为1: 2
查看答案和解析>>
科目:高中化学 来源:2015届江苏连云港市高三上第一次月考化学试卷(解析版) 题型:选择题
下列实验操作合理或能达到实验目的的是 ( )
A.用激光笔检验某KI溶液中是否溶有淀粉
B.配制一定物质的量浓度溶液时,容量瓶用蒸馏水洗涤后再用待装溶液润洗
C.向AgCl沉淀中滴加少量KI溶液,可说明Ksp(AgCl)<Ksp (AgI)
D.配制硫酸亚铁溶液,是将绿矾晶体溶于蒸馏水再加入一定量的铁粉
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
漂白粉的有效成分是
A.HClO B.NaClO C.Ca(ClO)2 D.CaCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com