
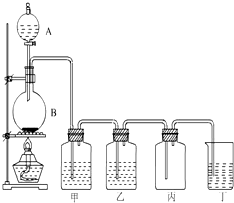
 如图为实验室制取氯气的装置图,请根据该图回答下列问题.
如图为实验室制取氯气的装置图,请根据该图回答下列问题.分析 (1)分析仪器形状和用途,A为分液漏斗,B为圆底烧瓶,A中加入的是浓盐酸,B中加入固体MnO2;
(2)(3)生成的氯气中含有水蒸气和氯化氢,通过饱和食盐水和浓硫酸除去得到干燥纯净的氯气;
(4)氯气有毒属于污染性气体不能排放到空气中需要通过氢氧化钠溶液吸收;
解答 解:(1)分析仪器形状和用途,A为加入液体的仪器为分液漏斗,B为反应容器为圆底烧瓶,A中盛放的是浓盐酸,B中加入的固体是二氧化锰,
故答案为:分液漏斗,圆底烧瓶,浓盐酸,二氧化锰;
(2)生成的氯气中含有氯化氢气体,可以通过饱和食盐水除去,甲装置盛放的物质是饱和食盐水,作用是除去氯气中的氯化氢气体,
故答案为:除去氯气中的氯化氢,饱和食盐水;
(3)生成的氯气中含有水蒸气,利用浓硫酸除去得到干燥纯净的氯气,乙装置盛放浓硫酸,作用是吸收氯气中的水蒸气,
故答案为:吸收氯气中的水蒸气,浓硫酸;
(4)氯气有毒属于污染性气体不能排放到空气中,需要通过氢氧化钠溶液吸收,氢氧化钠溶液作用是吸收剩余的氯气,防止污染空气,反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:吸收剩余的氯气,防止污染空气,Cl2+2NaOH=NaCl+NaClO+H2O;
点评 本题考查了实验室制备氯气的原理装置和除杂试剂选择,尾气处理方法,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 为提高成绩,可允许运动员在体育比赛中服用麻黄碱 | |
| B. | 毒品是指由于非医疗目的而反复使用使人产生成瘾性的药品,如吗啡、冰毒等 | |
| C. | 阿司匹林可以减轻感冒引起的头痛,但不能大量服用 | |
| D. | 用青霉素前一定要进行皮肤试验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制普通玻璃的原料主要是纯碱、石灰石和石英砂 | |
| B. | 玻璃在加热熔化时有固定的熔点 | |
| C. | 普通玻璃的主要成分中有硅酸钠、硅酸钙 | |
| D. | 盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅反应生成硅酸钠而使瓶塞与瓶口黏在一起 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配合物中心原子的电荷数和配位数均为6 | |
| B. | 该配合物可能是平面正方形结构 | |
| C. | Cl-和NH3分子均参与配位 | |
| D. | Cl-没有孤对电子,NH3有孤对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酯类物质是形成水果香味的主要成分 | |
| B. | 糖类物质都具有相同的官能团 | |
| C. | 油脂的皂化反应生成高级脂肪酸和甘油 | |
| D. | 蛋白质的水解产物都含有羧基和羟基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H3PO4?3H++PO43- | B. | BaSO4?Ba2++SO42- | ||
| C. | Al(OH)3?H2O+AlO2-+H+ | D. | NaHS?Na++H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向右移动 | B. | x+y>z | C. | B的转化率提高 | D. | C的体积分数增加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com