
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 氢氧化铝可与盐酸反应 | 氢氧化铝可用于治疗胃酸过多 |
| D | 冷的浓硝酸与铁不发生反应 | 可以用铁槽车储运浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.使溴水褪色体现了二氧化硫的还原性;
B.SiO2晶体对光具有全反射作用,能传递光信号;
C.胃酸中含有盐酸;
D.冷的浓硝酸与铁会发生钝化.
解答 解:A.单质溴与二氧化硫能发生氧化还原反应,二氧化硫可使溴水褪色体现了还原性,故A错误;
B.SiO2晶体对光具有全反射作用,能传递光信号,所以SiO2可用于制备光导纤维,故B错误;
C.胃酸中含有盐酸,氢氧化铝可与盐酸反应,所以氢氧化铝可用于治疗胃酸过多,故C正确;
D.冷的浓硝酸与铁会发生钝化,在铁的表面形成致密的氧化膜,能保护内部金属不要酸反应,所以可以用铁槽车储运浓硝酸,故D错误;
故选C.
点评 本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L醋酸钠溶液20ml与0.1mol/L盐酸10mL混合后的溶液中:c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | |
| B. | 物质的量浓度相等的①NH4Cl②(NH4)2SO4③NH4Al(SO4)2三种溶液中,c(NH4+)由大到小的顺序为:③>②>① | |
| C. | 浓度为O.lmol/L的①氨水、②C6H5ONa溶液、③Na2CO3溶液、④NaHCO3溶液,pH的大小顺序:①>④>③>②> | |
| D. | NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 用热的烧碱溶液洗去油污 | Na2CO3可直接和油污反应 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反 应生成CaCO3 |
| C | 施肥时,草木灰(有效成分为K2CO3)不能 与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低 肥效 |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,30 g乙烷气体中所含有的共价键数目为6NA | |
| B. | 标准状况下,0.4 g D2中所含中子的数目为0.2NA | |
| C. | 常温下,1 L pH=12的氨水溶液中含有NH4+数目为0.01NA | |
| D. | 标准状况下,盛有11.2 L NO2的密闭容器中氮原子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸;氢氧化铜与醋酸 | |
| B. | BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 | |
| C. | NaHCO3溶液与盐酸;Na2CO3与盐酸 | |
| D. | 石灰石与硝酸反应;石灰石与盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL1mol/L的氯化钠溶液 | B. | 75mL2mol/L的氯化铵溶液 | ||
| C. | 150mL3mol/L的氯化钾溶液 | D. | 75mL1mol/L的氯化亚铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
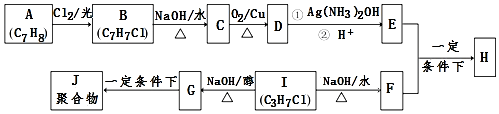
 .
. .
.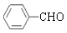 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$ +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
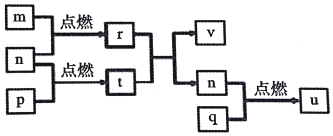 短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q,r、t、u是这些元素组成的二元化合物,其中u为形成酸雨的主要物质之一;25℃时,0.01mol•L-1的v溶液中:$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×1010.上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q,r、t、u是这些元素组成的二元化合物,其中u为形成酸雨的主要物质之一;25℃时,0.01mol•L-1的v溶液中:$\frac{c(O{H}^{-})}{c({H}^{+})}$=1.0×1010.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径的大小:W>Z>Y>X | |
| B. | Z分别与Y、W组成的化合物中化学键类型可能相同 | |
| C. | v能抑制水的电离而u能促进水的电离 | |
| D. | 粘有q的试管可用酒精洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com