
| 化学键 | H-H | C-O | C═O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
分析 (1)反应热=反应物总键能-生成物总键能;根据盖斯定律:反应②-反应①=反应③,反应热也进行相应的计算;
(2)反应①为CO(g)+2H2(g)?CH3OH(g),结合化学平衡常数的定义解答.
解答 解:(1)反应热=反应物总键能-生成物总键能,故△H1=1076kJ.mol-1+2×436kJ.mol-1-(3×413+343+465)kJ.mol-1=-99kJ.mol-1;
根据盖斯定律:反应②-反应①=反应③,故△H3=△H2-△H1=-58kJ.mol-1-(-99kJ.mol-1)=+41kJ.mol-1,
故答案为:-99;+41;
(2)反应①为CO(g)+2H2(g)?CH3OH(g),平衡常数为K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$,故答案为:K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$.
点评 本题考查化学平衡常数以及反应热有关计算,侧重考查学生分析计算能力,需要学生具备扎实的基础,注意把握化学平衡常数,难度中等.


科目:高中化学 来源: 题型:解答题
| 滴定 次数 | 待测溶液的体积(mL) | 0.100 0mol•L-1NaOH的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积(mL) | ||
| 第一次 | 20.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 20.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 20.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
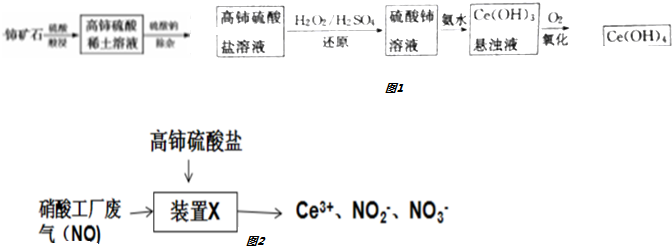
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
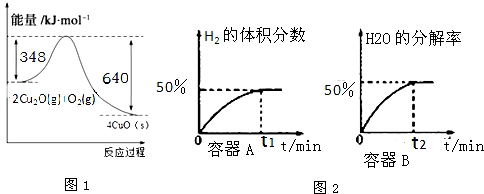
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
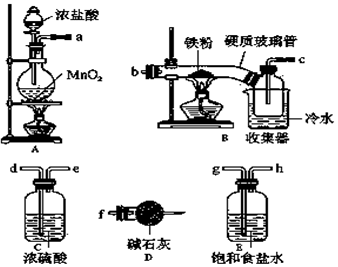
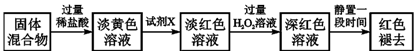
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,3.2 g O3所含电子数为1.2 NA | |
| B. | 标准状况下,2.24 L CCl4中含有的C-Cl键的数目为0.4 NA | |
| C. | 标准状况下,11.2 L NO与11.2 L O2混合所含原子数为2 NA | |
| D. | 将0.1 mol氯化铁溶于1 L水中,所得溶液含有0.1 NA Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 如图是病人输液用的葡萄糖(分子式为C6H12O6)注射液的标签上的部分内容.据标签所提供的信息,以下说法错误的是( )
如图是病人输液用的葡萄糖(分子式为C6H12O6)注射液的标签上的部分内容.据标签所提供的信息,以下说法错误的是( )| A. | 该注射液中葡萄糖的质量分数是5% | |
| B. | 葡萄糖的摩尔质量为180g•mol-1 | |
| C. | 该注射液的密度约为1g•mL-1 | |
| D. | 该注射液中葡萄糖的物质的量浓度约为0.014 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com