
分析 (1)依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸体积,据此选择量筒的规格;
(2)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(3)溶解固体时用玻璃棒搅拌加速固体溶解;移液时用玻璃棒引流;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)用18mol/L 浓硫酸配制100ml 3.0mol/L,设需要浓硫酸体积为V,则据溶液稀释过程中溶质的物质的量不变得:18mol/L×V=100mL×3.0mol/L,解得V=16.7mL;应选择20mL量筒;
故答案为:B;
(2)配制一定物质的量浓度溶液一般步骤:计算、量取、稀释、移液、洗涤、定容、摇匀,用到的仪器:玻璃棒、烧杯、量筒、胶头滴管、100mL 容量瓶;所以缺少的仪器:玻璃棒、100mL 容量瓶;
故答案为:玻璃棒、100mL 容量瓶;
(3)溶解固体时用玻璃棒搅拌加速固体溶解;移液时用玻璃棒引流,
故答案为:搅拌;引流;
(4)A.容量瓶用蒸馏水洗涤后残留有少量的水,对溶质的物质的量和溶液体积不会产生影响,溶液浓度不受影响;
故答案为:无影响;
B.所用过的烧杯、玻璃棒未洗涤,导致溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏小;
C.定容时俯视液面,导致溶液体积偏小,溶液浓度偏大,故答案为:偏大.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶使用方法和注意问题,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Ba(OH)2溶液与H2SO4溶液反应:Ba2++2H++2OH-+SO42-═BaSO4↓+2H2O | |
| C. | Na2CO3溶液与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | NH4Cl 溶液显酸性:NH4++H2O?NH3•H2O+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
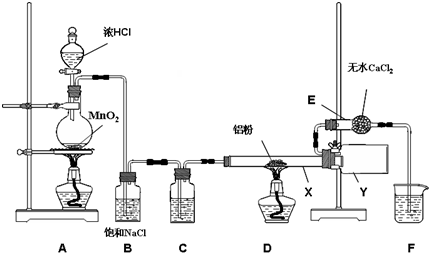
 2AlCl3
2AlCl3查看答案和解析>>
科目:高中化学 来源: 题型:解答题
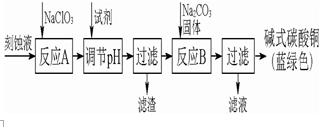 碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如图图所示.Cu2+、Fe2+、Fe3+生成沉淀的pH如表格所示:
碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如图图所示.Cu2+、Fe2+、Fe3+生成沉淀的pH如表格所示:| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加入适量NaCl溶液的方法除去Cu(NO3)2溶液中的AgNO3杂质 | |
| B. | 用洗气瓶中的NaOH溶液除去CO2气体中混有的HCl气体 | |
| C. | 分离FeCl3、KCl、BaSO4的固体混合物,应采用的一组试剂是:水、氢氧化钠、盐酸 | |
| D. | 先后添加石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原剂与氧化产物的物质的量之比为5:8 | |
| B. | 若氧化产物比还原产物多1.4mol则转移电子为1mol | |
| C. | 每生成1.6mol氮气,则有0.2molKNO3被氧化 | |
| D. | NaN3属于硝酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢是铁合金,钢的含碳量低于生铁,性能优于生铁 | |
| B. | 金属具有的物理通性是延展性、导热性、银白色光泽、导电性 | |
| C. | 符号Al既能表示铝元素,又能表示一个铝原子,还能表示铝单质 | |
| D. | 焊锡是锡铅合金,把铅加入锡中制成合金的主要目的是降低熔点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com