
25 ℃和1.01×105 Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.76 kJ/mol自发进行的原因是
A.是吸热反应 B.是放热反应
C.是熵减小的反应 D.熵增大效应大于能量效应
科目:高中化学 来源:2016-2017学年浙江省嘉兴市七校高一上期中化学试卷(解析版) 题型:选择题
下列分离方法中不正确的是( )
A.利用萃取方法用四氯化碳提取溴水中的溴单质
B.利用蒸馏的方法可以分离沸点相差较大的液体混合物
C.利用分液的方法分离酒精和水
D.利用结晶的方法除去KNO3中的氯化钾
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市红桥区高一上学期期中化学试卷(解析版) 题型:选择题
有以下四种物质:①标况下11.2L CO2 ②1g H2 ③1.204×1024个N2④4℃时18mLH2O,下列说法不正确的是( )
A.分子个数:③>④>①=② B.原子个数:③>④>①>②
C.体积:③>④>①=② D.质量 :③>①>④>②
:③>①>④>②
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市红桥区高一上学期期中化学试卷(解析版) 题型:选择题
如图实验装置或操作与微粒的大小无直接关系的是( )
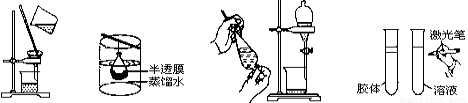
A. 过滤 B.渗析 C.萃取 D.丁达尔效应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:填空题
在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:SO2(g)+ NO2(g) SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________(填“增大” 、“不变”或“减小”);
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是___________mol/L;
(3)整个过程中,SO2的转化率由50%变为___________%,NO2的转化率由__________%变为___________%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将_______________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:选择题
下列事实能说明影响化学反应速率的主要因素是反应物自身性质的是
A.Cu能与浓硝酸反应,但不能与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C.N2与O2在常温、常压下不反应,放电时可反应
D.Fe与浓盐酸反应比与稀盐酸反应快
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:选择题
已知热化学方程式:SO2(g)+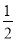 O2(g)
O2(g) SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上月考三化学试卷(解析版) 题型:选择题
下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是(  )
)
A.FeBr2与Cl2 B.Ba(OH)2与H2SO4
C.HCl与Na2CO3 D.NaHCO3与Ca(OH)2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
某溶液中由水电离产生的C(H+)=1.0×10-10mol/L,则下列各组离子在该溶液中肯定能大量共存的是
A、K+、Na+、HCO3-、Cl- B、Na+、K+、NO3-、Cl-
C、K+、Na+、S2-、NO3- D、Mg2+、Na+、SO32-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com