
| ���� | ���� | �Ϻ� | ��� | ���� | �Ͼ� | ���� | �麣 | ��ͷ | ���� | ���� | �ɶ� |
| ��Ⱦָ�� | 92 | 72 | 82 | 98 | 95 | 25 | 47 | 54 | 76 | 67 | 87 |
| ��Ҫ��Ⱦ�� | TSP | NOx | TSP | SO2 | TSP | TSP | TSP | TSP | |||
| �������� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� |
���� ��1������������õij���ӦΪ������Ⱦָ����͵ģ�
��2������Ϊ�������������ﵼ�£����������ᡢ����ȣ�SO2�����������������ʯ�ҷ�Ӧ����������ƣ����ձ�Ϊ����ƣ�
��3��NO��CO��Ӧ���ɵ����Ͷ�����̼����ת�����ɽ���������ת��Ϊ���������¿��������ߣ�
��� �⣺��1������������õij���ӦΪ������Ⱦָ����͵ģ��ɱ������ݿ�֪���ſ���������ã��ʴ�Ϊ�����ţ�
��2��������ָpH��5.6����ˮ���ɶ������������ﵼ�£����������ᡢ����ȣ������������������Ⱦָ����ߣ����γ����꣬SO2�����������������ʯ�ҷ�Ӧ����������ƣ����ձ�Ϊ����ƣ���Ӧ�Ļ�ѧ����ʽ CaO+SO2�TCaSO3��2CaSO3+O2�T2CaSO4��
�ʴ�Ϊ��pH��5.6�������ᡢ������죻 CaO+SO2�TCaSO3��2CaSO3+O2�T2CaSO4��
��3������Ϣ��֪������ת������ʹCO��NO��Ӧ������������Ϊ�����Ͷ�����̼���÷�ӦΪ2NO+2CO$\frac{\underline{\;����\;}}{\;}$N2+2CO2������ת��������ȱ������һ���̶�������˿�������ȣ�����ת������ʹ������ȼ�ռ�SO2��ת����ʹSO2ת������SO3��������ˮ��������ǿ��
�ʴ�Ϊ��2NO+2CO$\frac{\underline{\;����\;}}{\;}$N2+2CO2��ʹSO2ת������SO3��
���� ���⿼�鵪���������������ʼ�������Ⱦ��ע����Ϣ�ij�ȡ��Ӧ���ǽ����Ĺؼ�������ѧ����ȡ��Ϣ��������Ϣ�����Ŀ��飬����������ѧ�����õĿ�ѧ��������Ŀ�ѶȲ���


 ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgCl2�TMg2++2Cl- | B�� | Fe2��SO4��3�T2Fe3++3SO42- | ||
| C�� | NaHCO3�TNa++H++CO32- | D�� | KHSO4�TK++H++SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
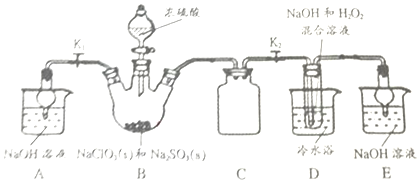
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+SO32-Cl- | B�� | Cu2+SO42-NO3- | C�� | Na+K+I- | D�� | Ag+Br-Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Ũ������Ũ����һ�����ڿ����г��ְ��� | |
| B�� | �������ֽ�����ȷֽ������ͬ������NO2��O2��H2O | |
| C�� | NO2��ˮ��Ӧ��HNO3���ɣ�����NO2������ | |
| D�� | �����������Ӧ���ȱ��ֳ������ԣ��ֱ��ֳ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2��NO2 | B�� | N2��NH3 | C�� | NO��NO2 | D�� | NH3��NO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
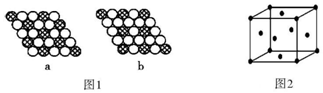 ���������е� 18 ��Ԫ�ؾ�����Ҫ����;��
���������е� 18 ��Ԫ�ؾ�����Ҫ����;���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢ� | B�� | �٢ڢۢ� | C�� | �ڢܢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com