
【题目】下列反应属于加成反应的是
A. 乙烯使溴水褪色
B. 甲烷与氯气在光照条件下的反应
C. 苯和液溴在铁作催化剂的条件下反应
D. 乙醇与氧气在铜作催化剂及加热条件下的反应
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】某温度下,密闭容器中,发生如下可逆反应:2E(g) ![]() F(g)+xG(g);ΔH<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为0.5a mol·L-1;若E的起始浓度改为2a mol·L-1,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是( )
F(g)+xG(g);ΔH<0。若起始时E浓度为a mol·L-1,F、G浓度均为0,达平衡时E浓度为0.5a mol·L-1;若E的起始浓度改为2a mol·L-1,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是( )
A.若x=1,容器体积保持不变,新平衡下E的体积分数为50%
B.升高温度时,正反应速率加快、逆反应速率减慢
C.若x=2,容器体积保持不变,新平衡下F的平衡浓度为0.5a mol·L-1
D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物顺序排列的是( )
A. 食醋、液态氧、碘酒 B. 生石灰、白磷、熟石灰
C. 干冰、铁、盐酸 D. 空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,2体积AB2气体和1体积B2气体化合生成2体积气态化合物,则该化合物的化学式为( )
A.AB3
B.AB2
C.A3B
D.A2B3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氧化碳是一种用途广泛的化工基础原料。有机物加氢反应中镍是常用的催化剂。但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:
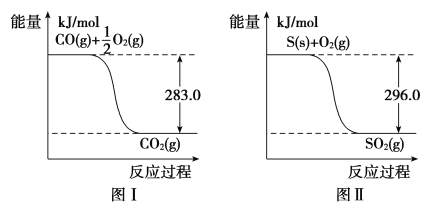
则:(1)① 不用通入O2氧化的方法除去CO的原因是____________________。
②SO2(g)+2CO(g)===S(s)+2CO2(g) ΔH=________。
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g)![]() CO2(g)+H2(g),已知420 ℃时,该反应的化学平衡常数K=9。如果反应开始时,在2 L的密闭容器中充入CO和H2O的物质的量都是0.60 mol,5 min末达到平衡,则此时CO的转化率为________,H2的平均生成速率为________ mol·L-1·min-1。
CO2(g)+H2(g),已知420 ℃时,该反应的化学平衡常数K=9。如果反应开始时,在2 L的密闭容器中充入CO和H2O的物质的量都是0.60 mol,5 min末达到平衡,则此时CO的转化率为________,H2的平均生成速率为________ mol·L-1·min-1。
(3)为减少雾霾、降低大气中有害气体含量, 研究机动车尾气中CO、NOx及CxHy的排放量意义重大。机动车尾气污染物的含量与空/燃比 (空气与燃油气的体积比)的变化关系示意图如图所示:
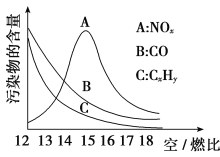
①随空/燃比增大,CO和CxHy的含量减少的原因是_______________________。
②当空/燃比达到15后,NOx减少的原因可能是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质,A元素的阳离子为第三周期半径最小的离子。反应过程中生成的水及其他产物已略去,请回答以下问题:

(1)B________, F_______,H_______。(填化学式)
(2)写出A与B反应的化学方程式:_______________________________。
(3)写出H在空气中转化成I的反应的化学方程式:_________________。
(4)5.4 g A的单质与100 mL 3 mol/L HCl溶液反应,可生成标况下的气体_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年5月17日新疆电视台(午间新闻)报道:我国新增阿勒泰大气背景监测点。这标志着气候条件独特、空气质量优良的新疆阿勒泰市已成为我国第8个国家大气背景监测点。监测点安装的监测设备可监测日常二氧化硫、二氧化氮、一氧化氮等污染物。
(1)NO分子因污染空气而臭名昭著, NO对环境的危害在于________(填编号)。
A.破坏臭氧层 B.高温下能使一些金属氧化
C.造成酸雨 D.与人体血红蛋白结合
(2)SO2被称为“空中死神”,其对环境的危害常表现为形成“酸雨”。工业上常用生石灰来处理煤炭中的SO2,这是利用了SO2属于__________氧化物的性质。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。近年来,有人提出了一种利用电解饱和氯化钠溶液(2NaCl+2H2O===2NaOH+Cl2+H2)循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是________________________。
②写出反应Ⅰ的离子方程式:________________________________。
(3)氟利昂(如CCl2F2)可在光的作用下分解,产生氯原子,氯原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应如下:
![]() 总反应:2O3===3O2
总反应:2O3===3O2
在上述臭氧变成氧气的过程中,Cl是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com