
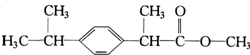
 某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )
某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
分析 有机物X含有的官能团为酯基,所以具有酯的性质,
①根据相似相溶原理分析,有机溶质易溶于有机溶剂.
②能和溴水反应的有碳碳双键或三键、含酚羟基的苯环等.
③能和酸性高锰酸钾反应的有碳碳双键或三键、苯环上的支链等.
④X的水解产物是羧酸和醇,根据醇的结构分析判断.
解答 解:①X是有机物,根据相似相溶原理知,X难溶于水,易溶于有机溶剂,故①正确;
②因为X既不含碳碳双键或三键又不含酚羟基的苯环,所以X不能跟溴水反应,故②错误;
③因为X的苯环上含有支链,所以X能被酸性高锰酸钾氧化而使酸性高锰酸钾溶液褪色,故③正确;
④X的水解产物是羧酸和醇,羧酸不能发生消去反应;甲醇只有一个碳原子,所以也不能发生消去反应,故④错误;
故选B.
点评 本题考查了有机物结构与性质,题目难度中等,明确有机物分子中含有官能团类型为解答关键,注意掌握常见有机物结构与性质,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 用A浓度表示该反应速率为1.6 mol/(L•min) | |
| B. | 若使容器体积变为1 L,则B的物质的量一定减小 | |
| C. | 达到平衡,测得放出热量为x kJ,则x=Q | |
| D. | 若向容器再充入1 mol C,重新达到平衡,A的体积分数保持不变,则B为气态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
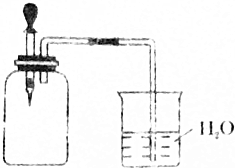 如图所示,将1molCH4与1molCl2混合后充入集气瓶内,置于光亮处,让混合气体缓慢地反应一段时间.
如图所示,将1molCH4与1molCl2混合后充入集气瓶内,置于光亮处,让混合气体缓慢地反应一段时间.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4O | B. | C2H5OH | C. | CH3CHO | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
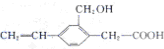
| A. | 该有机化合物的分子式为C11H10O3 | |
| B. | 该有机化合物能发生取代反应、加成反应和加聚反应 | |
| C. | 1mol该有机化合物分别消耗Na、NaOH和NaHCO3的物质的量之比为2:2:1 | |
| D. | 该有机化合物与 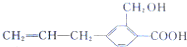 互为同系物 互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com