
·ÖĪö A£®·ÖĄė»„²»ĻąČܵÄĘūÓĶŗĶĖ®£¬æÉĶعż·ÖŅŗ·½·Ø£»
B£®ŻĶČ”¼ĮµÄєȔŌŌņŹĒĮ½ÖÖČܼĮ»„²»ĻąČÜ£»
C£®ĒāŃõ»ÆÄĘæÉÓė“ÉŪįŪö£ØSiO2£©·“Ӧɜ³É¹čĖįÄĘŗĶĖ®£»
D£®Fe£ØOH£©3½ŗĢåÓŠ¶”“ļ¶ūŠ§Ó¦£¬CuSO4ČÜŅŗĪŽ£»
E£®·ÖŅŗŹ±£¬±ÜĆāÉĻĻĀ²ćŅŗĢå»ģŗĻ£®
½ā“š ½ā£ŗA£®ĘūÓĶŗĶĖ®»„²»ĻąČÜ£¬æÉĶعż·ÖŅŗ·½·Ø·ÖĄė£¬¹ŹAÕżČ·£»
B£®ŻĶČ”¼ĮµÄєȔŌŌņŹĒĮ½ÖÖČܼĮ»„²»ĻąČÜ£¬¾Ę¾«Ņ×ČÜÓŚĖ®£¬¹ŹB“ķĪó£»
C£®¼ÓČČČŪ»ÆŹ±£¬ĒāŃõ»ÆÄĘ¹ĢĢåæÉÓė“ÉŪįŪö£ØSiO2£©·“Ӧɜ³É¹čĖįÄĘŗĶĖ®£¬Ņ×µ¼ÖĀŪįŪöÕØĮŃ£¬¹ŹC“ķĪó£»
D£®ÄÜÓƶ”“ļ¶ūŠ§Ó¦¼ų±šFe£ØOH£©3½ŗĢåŗĶCuSO4ČÜŅŗ£¬Fe£ØOH£©3½ŗĢåÓŠ¶”“ļ¶ūŠ§Ó¦£¬CuSO4ČÜŅŗĪŽ£¬¹ŹDÕżČ·£»
E£®·ÖŅŗŹ±£¬±ÜĆāÉĻĻĀ²ćŅŗĢå»ģŗĻ£¬Ōņ·ÖŅŗĀ©¶·ÖŠµÄĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö£¬ÉĻ²ćŅŗĢå“ÓÉĻæŚµ¹³ö£¬¹ŹEÕżČ·£»
¹Ź“š°øĪŖ£ŗA”¢D”¢E£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧŹµŃé·½°øµÄĘĄ¼Ū£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ»ģŗĻĪļ·ÖĄėĢį“æ·½·Ø”¢ŹµŃé²Ł×÷ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬עŅāŹµŃéµÄĘĄ¼ŪŠŌ·ÖĪö£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4LSO3ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬17gNH3 Ėłŗ¬µÄŌ×ÓŹżÄæĪŖ4NA | |
| C£® | 1 molCl2ÓėH2OĶźČ«·“Ó¦£¬×ŖŅĘ2NAøöµē×Ó | |
| D£® | 0.1mol/LNa2CO3ČÜŅŗÖŠŗ¬ÓŠµÄNa+ŹżÄæĪŖ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³żČ„HClČÜŅŗÖŠµÄÉŁĮæH2SO4£¬æɼÓČėŹŹĮæBa£ØNO3£©2ČÜŅŗŗó¹żĀĖ | |
| B£® | ³żČ„Ģś·ŪÖŠµÄÉŁĮæĀĮ·Ū£¬æɼÓČėŹŹĮæĻ”ŃĪĖįŗó¹żĀĖ | |
| C£® | ³żČ„FeCl3ČÜŅŗÖŠµÄÉŁĮæCuCl2£¬æɼÓČėŹŹĮæĢś·Ūŗó¹żĀĖ | |
| D£® | ³żČ„Na2CO3¹ĢĢåÖŠµÄÉŁĮæNaHCO3£¬æɽ«¹ĢĢå¼ÓČČÖĮŗćÖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeO | B£® | Al£ØOH£©3 | C£® | Na2CO3 | D£® | NaHCO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņŹĒŅ»ÖÖŅ×ČÜÓŚ¾Ę¾«µÄ»ĘÉ«¾§Ģå | |
| B£® | SO2ČÜÓŚĖ®Éś³ÉH2SO4 | |
| C£® | æÉÓĆĒāŃõ»ÆÄĘČÜŅŗ“¦Ąķŗ¬ÓŠSO2µÄĪ²Ęų | |
| D£® | ÅØH2SO4²»ĪČ¶Ø£¬¹āÕÕŅ×·Ö½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĢśĘ¬ŗĶĻ”ĮņĖį·“Ó¦ÖĘČ”ĒāĘųŹ±£¬øÄÓĆ9.8%µÄÅØĮņĖįæÉŅŌ¼Óæģ²śÉśĒāĘųµÄĖŁĀŹ | |
| B£® | 10.0 mL 2 molL -1µÄŃĪĖįøśŠæʬ·“Ó¦£¬¼ÓČėŹŹĮæµÄĀČ»ÆÄĘČÜŅŗ£¬·“Ó¦ĖŁĀŹ²»±ä | |
| C£® | SO 2µÄ“ß»ÆŃõ»ÆŹĒŅ»øö·ÅČȵķ“Ó¦£¬ĖłŅŌÉżøßĪĀ¶Č£¬·“Ó¦ĖŁĀŹ¼õĀż | |
| D£® | Ęū³µĪ²ĘųÖŠµÄNOŗĶCOæÉŅŌ»ŗĀż·“Ӧɜ³ÉN2ŗĶCO2£¬¼õŠ”Ń¹Ē棬·“Ó¦ĖŁĀŹ¼õĀż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | c£ØB2-£©+c£ØHB-£©+c£ØH2B£©=0.1 mol/L | B£® | c£ØNa+£©+c£ØH+£©=c£ØOH-£©+c£ØHB-£©+c£ØB2-£© | ||
| C£® | c£ØOH-£©=c£ØH+£©+c£ØHB-£© | D£® | c£ØNa+£©=2c£ØB2-£©+c£ØHB-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
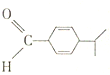
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com