
【题目】将 Na2CO3 和 Na2S 按 1∶2 的物质的量之比配成溶液,再通入 SO2,可制取 Na2S2O3,同时放出CO2。在该反应中( )
A.被氧化与被还原的原子个数比为 2∶1
B.相同条件下,每吸收 1 m3 SO2 就会放出 2.5 m3 CO2
C.每 1 mol Na2S 反应,则生成的 Na2S2O3 为 1.5 mol
D.若有 106 g Na2CO3 发生反应,反应中转移的电子的物质的量为 4 mol
【答案】C
【解析】
工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2,其反应方程式为2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,反应在Na2S 中S元素的化合价从-2价升高到+2价,SO2中S的化合价从+4价降低到+2价,据此分析。
A. 由反应方程式中S元素的化合价变化可知,硫元素既被氧化又被还原,被氧化与被还原的原子个数比为1∶2,故A错误;
B.2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2中SO2与CO2的物质的量之比为4∶1,相同条件下的气体的物质的量之比等于气体的体积之比,每吸收 4m3 SO2 就会放出1 m3 CO2,故B错误;
C. 反应中Na2S和Na2S2O3的物质的量之比为2∶3,每 1 mol Na2S 反应,则生成的 Na2S2O3 为 1.5 mol,故C正确;
D. 反应方程式为2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,反应在Na2S 中S元素的化合价从-2价升高到+2价,SO2中S的化合价从+4价降低到+2价,若有 106 g Na2CO3 发生反应,则碳酸钠的物质的量=![]() =
=![]() =1mol,根据方程式1mol Na2CO3反应时转移8mol电子,故D错误;
=1mol,根据方程式1mol Na2CO3反应时转移8mol电子,故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。如图是废旧钻酸锂(LiCoO2)(含少量铁、铝、铜等元素的化合物)回收工艺流程:
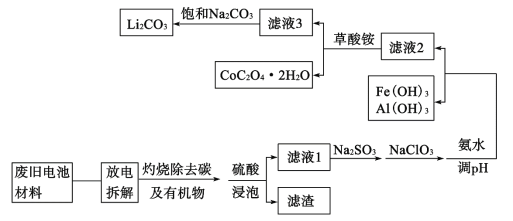
(1)“拆解”前需进入“放电”处理的目的是__;用食盐水浸泡是放电的常用方法,浸泡放电过程中产生的气体主要有__。
(2)上述流程中将CoO2-转化为Co3+的离子方程式为__。
(3)滤液1中加入Na2SO3的主要目的是__;加入NaClO3的主要目的是__。
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:

根据图沉钴时应控制n(C2O42-):n(Co2+)比为__,温度控制在__℃左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】举世闻名的侯氏制碱法的工艺流程如下图所示,下列说法正确的是
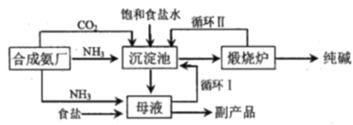
A.往母液中加入食盐的主要目的是使NaHCO3更多的析出
B.从母液中经过循环Ⅰ进入沉淀池的主要是Na2CO3、NH4Cl和氨水
C.沉淀池中反应的化学方程式:2NH3+CO2+2NaCl+H2O=2NH4Cl+Na2CO3
D.设计循环Ⅱ的目的是使原料二氧化碳利用率大大提升
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院某课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法中正确的是( )
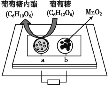
A. a极为正极
B. 随着反应不断进行,负极区的pH不断增大
C. b极电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
D. 消耗0.01mol葡萄糖,电路中转移0.02mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中常含 Ca2+、Mg2+、SO42-以及泥沙等杂质,一种制备精盐的实验方案及步骤如下(用于沉淀的试剂饱和 Na2CO3 溶液、BaCl2 溶液、NaOH 溶液均稍过量):
![]()
(1)若试剂①选用 NaOH 溶液,则试剂②产生的沉淀的化学式为 ___________。判断滴加试剂③ 已过量的方法是:__________。
(2)操作Ⅱ为___________。溶液丙中,溶质除 NaCl 外还含有____________(填化学式)等。
(3)食用盐常在精盐中加入 KIO3。为了检验实验中是否含 KIO3,可以用以下反应进行:KIO3+5KI+3H2SO4![]() 3I2+3K2SO4+3H2O。
3I2+3K2SO4+3H2O。
①用双线桥分析以上反应中电子转移的方向和数目:_____。
②反应中氧化剂与还原剂的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
A. 分子总数为NA的二氧化硫和二氧化碳混合气体中含有的原子数为3NA
B. 任何条件下,20 L 氧气含有的分子数都不可能为NA
C. 在标准状况下,2 g氖气含有NA个氖原子
D. 物质的量相等的任何气体中都含有相同的原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有MgCl2,从海水中提取镁,正确的方法是
A.海水![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B.海水![]() MgCl2溶液→ MgCl2(熔融)
MgCl2溶液→ MgCl2(熔融)![]() Mg
Mg
C.海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D.海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液 → MgCl2(熔融)
MgCl2溶液 → MgCl2(熔融)![]() Mg
Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A 0.2 mol在氧气中充分燃烧后,生成化合物B、C各1.2 mol,试完成下列问题:
(1)烃A的分子式为____。
(2)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为_____。
(3)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A所有可能的结构简式分别为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com