
| A、盐酸、食盐、水银 |
| B、水玻璃、冰、火碱 |
| C、纯碱、铜绿、漂白粉 |
| D、干冰、液氨、酒精 |


科目:高中化学 来源: 题型:
| A、Al2(SO4)3溶液滴加氨水产生白色胶状沉淀:Al3++3OH-═Al(OH)3↓ |
| B、90℃时,测得纯水中c(H+)?c(OH-)═3.8×10-13:H2O(l)?H+(aq)+OH-(aq)△H<0 |
| C、FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ |
| D、碳酸钠溶液滴入酚酞变红:CO32-+2H2O?H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将0.2 mol?L-1的某一元酸HA溶液和0.1 mol?L-1 NaOH溶液等体积混合后,混合液pH大于7,则反应后的混合液:2c(OH一)+c(A-)═2c(H+)+c(HA) |
| B、某溶液中存在的离子有Cl-、OH-、NH4+、H+,则离子浓度不一定是c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、某物质的溶液中由水电离出的c(H+)=1×10-a mol?L-1,若a>7时,则该溶液的pH一定为14-a |
| D、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:2c(R2-)+c(HR一)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
| A、该反应是吸热反应 |
| B、该反应的平衡常数随温度的升高而增大 |
| C、压强升高时平衡常数也随之增大 |
| D、该反应的平衡常数随温度的升高而减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
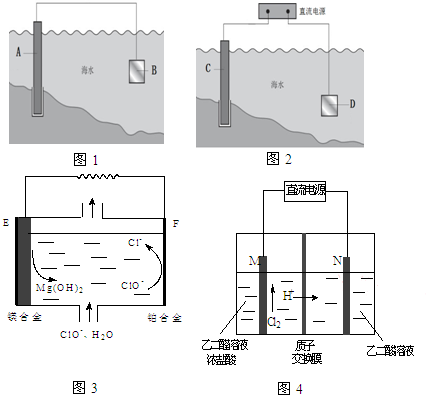 电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛.
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:
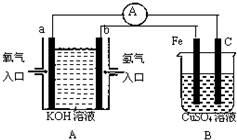 根据如图所示装置回答问题:
根据如图所示装置回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| B、常温下,pH≈5.5的0.1mol/LNaHC2O4溶液:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
| C、0.1mol/LNaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) |
| D、室温下,向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com