
【题目】下列各组的两物质作用时,反应条件或反应物用量的改变对生成物没有影响的是
A.Na2O2与CO2B.Na与O2C.NaOH与AlCl3D.C与O2
【答案】A
【解析】
A.过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+CO2=2Na2CO3+O2↑,该反应与反应条件或反应物用量的改变对生成物无关,故A正确;
B.常温下钠与氧气反应生成氧化钠,反应的化学方程式为4Na+O2=2Na2O,点燃或加热时钠与氧气反应生成过氧化钠,反应的化学方程式为2Na+O2![]() Na2O2,反应产物与反应温度有关,故B错误;
Na2O2,反应产物与反应温度有关,故B错误;
C.氯化铝与少量氢氧化钠溶液反应生成氢氧化铝沉淀和氯化钠,反应的化学方程式为AlCl3+3NaOH=Al(OH)3↓+3NaCl,氯化铝与过量氢氧化钠溶液反应生成偏铝酸钠、氯化钠和水,AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,反应产物与相对用量有关,故C错误;
D.碳在氧气中不完全燃烧生成一氧化碳,反应的化学方程式为2C+O2=2CO,碳在氧气中完全燃烧生成二氧化碳,反应的化学方程式为C+O2=CO2,反应产物与相对用量有关,故D错误;
故选A。


科目:高中化学 来源: 题型:
【题目】已知钍![]() Th的原子可发生下列放射性变化:
Th的原子可发生下列放射性变化: ![]() Th→
Th→![]() X+
X+![]() He,生成的X是与Mg同主族的一种元素的原子,下列对X的推断错误的是
He,生成的X是与Mg同主族的一种元素的原子,下列对X的推断错误的是
A. X的氢氧化物是一种强碱B. X元素位于第六周期
C. X的碳酸盐难溶于水D. X的最高化合价为+2价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法错误的是( )
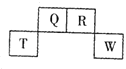
A.气态氢化物稳定性:R>Q
B.元素T的离子半径>元素R的离子半径
C.与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键
D.Q可形成多种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列萃取与分液结合进行的操作(用![]() 作萃取剂,从碘水中萃取磺)错误的是( )
作萃取剂,从碘水中萃取磺)错误的是( )
A.碘水和![]() 加入分液漏斗后,盖好玻璃塞,右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来振荡
加入分液漏斗后,盖好玻璃塞,右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来振荡
B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)
C.打开分液漏斗的活塞,使下层液体全部沿盛接液体的烧杯内壁慢慢流出
D.最后继续打开活塞,另用容器盛接并保存上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容条件下,1 mol SiHCl3发生如下反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)x(SiCl4),k正、k逆分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
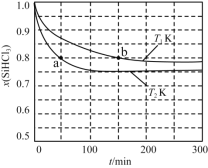
A. 该反应为放热反应,v正,a<v逆,b
B. 化学平衡状态时2v消耗(SiHCl3)=v消耗(SiCl4)
C. 当反应进行到a处时,v正/v逆=16/9
D. T2 K时平衡体系中再充入1 mol SiHCl3,平衡正向移动,x(SiH2Cl2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)A+和B-的电子层结构都与氩相同,A+的结构示意图为___;
(2)碳原子核外有___种能量不同的电子,分布在___个轨道中;
(3)鉴别碳原子可以利用其激发态原子跃迁到基态所形成的特征___(吸收或发射)光谱;
(4)水、SiO2、硫三种物质沸点由大到小的顺序为___;
(5)下列变化:H-(g)=H(g) +e-吸收的能量为73kJ·mol-1,H(g)=H+(g)+e-吸收的能量为1311kJ·mol-1,则氢负离子H-的第一电离能为___;
(6)短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。四种原子半径的由大到小顺序___(元素符号表示),能证明W、Z两元素非金属性强弱的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大,X阴离子的电子数与Y原子的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的两种元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的元素名称为___________;五种元素的原子半径从小到大的顺序是(用元素符号表示)______________。
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,用电子式表示A的形成过程_______________,B的结构式为________。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为________。
(4)一定条件下,M与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组按下列路线合成药物诺氟沙星:
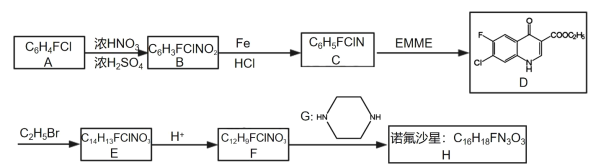
已知:
试剂EMME为C2H5OCH=C(COOC2H5)2,在适当条件下,可由C生成D。
②![]()
③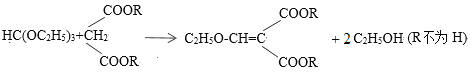
请回答:
(1)根据以上信息可知诺氟沙星的结构简式_____。
(2)下列说法不正确的是_____。
A.B到C的反应类型为取代反应
B.EMME可发生的反应有加成,氧化,取代,加聚
C.化合物E不具有碱性,但能在氢氧化钠溶液中发生水解
D.D中两个环上的9个C原子可能均在同一平面上
(3)已知:RCH2COOH![]() ,设计以化合物HC(OC2H5)3、C2H5OH合成EMME的合成路线(用流程图表示,无机试剂任选)_____。
,设计以化合物HC(OC2H5)3、C2H5OH合成EMME的合成路线(用流程图表示,无机试剂任选)_____。
(4)写出C→D的化学方程式______。
(5)写出化合物G的同系物M(C6H14N2)同时符合下列条件的同分异构体的结构简式:____
①1H-NMR谱表明分子中有4种氢原子,IR谱显示含有N-H键,不含N-N键;
②分子中含有六元环状结构,且成环原子中至少含有一个N原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl2具有独有的脱色能力,适用于印染、造纸行业的污水处理。FeCl3在加热条件下遇水剧烈水解。FeCl3和FeCl2均不溶于C6H5Cl、C6H4Cl2、苯。回答下列问题:
(1)由FeCl3.6H2O制得干燥FeCl2的过程如下:
i.向盛有FeCl3.6H2O的容器中加入过量SOCl2(液体,易水解),加热,获得无水FeCl3。
ii.将无水FeCl3置于反应管中,通入一段时间的氢气后再加热,生成FeCl2。
①FeCl3.6H2O中加入SOCl2获得无水FeCl3的化学方程式为__________________。(已知该反应为非氧化还原反应)
②使用NH4SCN可以检验 ii中FeCl3是否含完全转化,请写出离子反应方程式_____________。
(2)利用反应2FeCl3 + C6H5Cl ![]() 2FeCl2+ C6H4Cl2 +HCl↑,制取无水FeCl2。在三颈烧瓶中加入无水氯化铁和过量的氯苯,控制反应温度在一定范围内加热3 h,冷却、分离、提纯得到粗产品,实验装置如图。(加热装置略去)
2FeCl2+ C6H4Cl2 +HCl↑,制取无水FeCl2。在三颈烧瓶中加入无水氯化铁和过量的氯苯,控制反应温度在一定范围内加热3 h,冷却、分离、提纯得到粗产品,实验装置如图。(加热装置略去)

①仪器B的名称是_________ ;C的试剂名称是________。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经______、_______、干燥后,得到FeCl2粗产品。
③该装置存在的不足之处是__________________________。
(3)粗产品中FeCl2的纯度测定。
①取a g粗产品配制成100 mL溶液;②用移液管移取所配溶液5.00mL,放入500 mL锥形瓶内并加水至体积为200mL;③用0.100 mol·L-1酸性KMnO4标准溶液滴定,终点时消耗酸性KMnO4标准溶液V mL。若已知消耗酸性高锰酸钾溶液为VmL,所配溶液的密度ρ(FeCl2)=kV ,密度的单位为g·L-1,则k=___________g·L-1·mL-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com