
 NaCl��NaClO�����������¿ɷ�����Ӧ��ClO-+Cl-+2H+�TCl2��+H2O��ijѧϰС�����о�����Һ����Ҫ�ɷ�ΪNaCl��NaClO���ı��������
NaCl��NaClO�����������¿ɷ�����Ӧ��ClO-+Cl-+2H+�TCl2��+H2O��ijѧϰС�����о�����Һ����Ҫ�ɷ�ΪNaCl��NaClO���ı��������| �����Լ� | Ԥ������ͽ��� |
| ���Թ�A�м�������1.0mol/LK������Һ�� �Թ�B�м�1%Ʒ����Һ�� �Թ�C�мӢڳ���ʯ��ˮ�� | ��A����Һ����ɫ��B����Һ����ɫ��C����Һ����ǣ�������Һ���ֱ��ʣ� ����A����Һ����ɫ��B����Һ����ɫ���ޱ仯����C����Һ������ǣ��ޱ仯����������Һδ���ʣ�������Һδ���ʣ� ����A����Һ������ɫ���ޱ仯����B����Һ����ɫ���ޱ仯����C����Һ�����������Һ��ȫ���ʣ�������Һ��ȫ���ʣ� |
���� ��1��̼������Աȴ�����ǿ�����������������̼��ˮ��Ӧ����̼������������
��2����������Һ�����ᷴӦ���ɵ��������Ƿ���������������̼�������ж�����Һ�ı������������������1.0mol/L��KI������Һ��KI������Һ������˵�������к������������������̼�ù�����ʯ��ˮ������ʯ��ˮ����ǣ�˵�������к��ж�����̼��ע�������Ĵ��ڻ���Ŷ�����̼�ļ��飬��KI������Һ�����������⣬�����ȥ���������ã�װ��B���ڼ��������Ƿ������
��3��������KMnO4��Һ����ǿ�����ԣ����Ը�ʴ��Ƥ�ܣ�Ӧװ����ʽ�ζ����У�
�۸�������KMnO4��Һ���������5Na2SO3��2KMnO4����ʣ����������ƣ�����������������Ʒ�Ӧ���������ƣ��ٸ���NaClO��Na2SO3�������������Ƶ����ʵ���������c=$\frac{n}{V}$��������Һ��NaClO��Ũ�ȣ�
��� �⣺��1��̼������Աȴ�����ǿ�����������������̼��ˮ��Ӧ����̼������������ᣬ��Ӧ����ʽΪNaClO+CO2+H2O=NaHCO3+HClO��
�ʴ�Ϊ��NaClO+CO2+H2O=NaHCO3+HClO��
��2����������Һ�����ᷴӦ���ɵ��������Ƿ���������������̼�������ж�����Һ�ı��������
װ��A�����Ǽ�����������1.0mol/L��KI������Һ��װ��B���������Ƿ������װ��C���������̼���ù�����ʯ��ˮ��
��A����Һ����ɫ��B����Һ����ɫ��C����Һ����ǣ�������Һ���ֱ��ʣ�
��A����Һ����ɫ��B����Һ����ɫ���ޱ仯����C����Һ������ǣ��ޱ仯����������Һδ���ʣ�
��A����Һ������ɫ���ޱ仯����B����Һ����ɫ���ޱ仯����C����Һ�����������Һ��ȫ���ʣ�
�ʴ�Ϊ��
| �����Լ� | Ԥ������ͽ��� |
| ��1.0mol/L K������Һ �ڳ���ʯ��ˮ | ����A����Һ����ɫ��B����Һ����ɫ���ޱ仯����C����Һ������ǣ��ޱ仯����������Һδ���� ����A����Һ������ɫ���ޱ仯����B����Һ����ɫ���ޱ仯����C����Һ�����������Һ��ȫ���� |
���� ���⿼��Ԫ�ػ��������ʡ���������ɵ�̽����ơ����ʵļ��顢�ζ���Ӧ�������ȣ���Ŀ�Ѷ��еȣ��Ƕ���ѧ֪ʶ���ۺ�Ӧ�ã�ע��֪ʶ�����������⣬��3���м������巴Ӧ������ζ���ԭ���ǽ���ؼ���������Ҫѧ���������õ��������ʣ�


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ԫ�غͷǽ���Ԫ���ڲ�ͬ�������ж����ܳʲ�ͬ�Ļ��ϼ� | |
| B�� | ͬһԪ�ز����ܼȱ��ֽ����ԣ��ֱ��ַǽ����� | |
| C�� | ������Ķ�����Ԫ���γ���ۻ�����ʱ������㶼�ﵽ8�����ȶ��ṹ | |
| D�� | ͬһ�����Ԫ�أ���ѧ����Ҳ���ܲ���ܴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol18O2����������Ϊ16NA | |
| B�� | 100mL pH=3�Ĵ�����Һ�У���������ĿС��10-4NA | |
| C�� | 0.5mol���ֱ��������ռ�����ᷴӦת�Ƶĵ�������ȣ���Ϊ1.5NA | |
| D�� | ��״���£�11.2L SO3����������Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
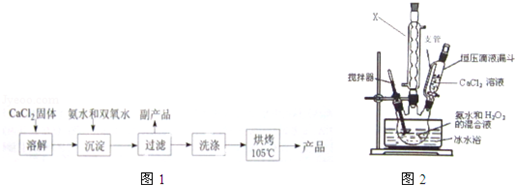
| ʵ����� | ��1�� | ��2�� | ��3�� | ��4�� |
| ����KMnO4���/mL | 19.98 | 20.02 | 20.20 | 20.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������Ϊ37����ԭ�ӣ�${\;}_{37}^{17}$Cl | |
| B�� | ��������ӵĵ���ʽ��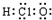 | |
| C�� | ���������Ľṹ��ʽ�� | |
| D�� | Al��OH��3�ĵ��룺H++AlO2-+H2O?Al��OH��2?Al3++3OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
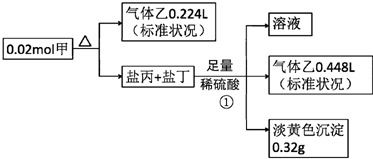
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ��������������Ӧ | B�� | �ϳɰ���Ӧ | ||
| C�� | �ð����ϳ����� | D�� | ����þ�ڵ�����ȼ������Mg3N2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
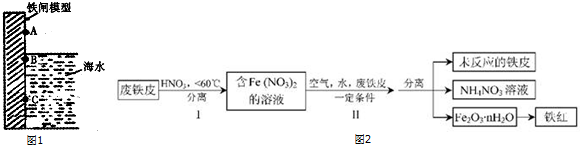
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com