
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |


科目:高中化学 来源:不详 题型:单选题
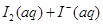

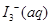 某I2、、KI混合溶液中,
某I2、、KI混合溶液中,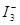 的物质的量浓度c(
的物质的量浓度c(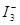 )与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是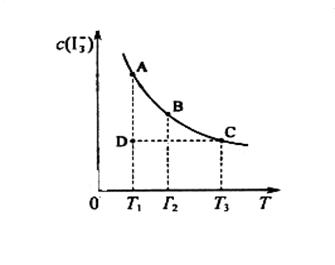
A.反应 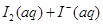  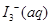 △H>0 △H>0 |
B.若温度为 ,反应的平衡常数分别为 ,反应的平衡常数分别为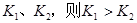 |
C.若反应进行到状态D时, |
| D.状态A与状态B相比,状态A的c(I2)大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 PCl5(g),达平衡时PCl5为0.4mol,如果此时移走1.0molPCl3和0.5molCl2,在 相同温度下再次达到平衡时,PCl5的物质的量为 ( )
PCl5(g),达平衡时PCl5为0.4mol,如果此时移走1.0molPCl3和0.5molCl2,在 相同温度下再次达到平衡时,PCl5的物质的量为 ( )| A.0.4mol |
| B.0.2mol |
| C.小于0.2mol |
| D.大于0.2mol,小于0.4mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4NO(g)+6H2O(g) ΔH<0若此反应起始的物质的量相同,则下列关系图正确的是
4NO(g)+6H2O(g) ΔH<0若此反应起始的物质的量相同,则下列关系图正确的是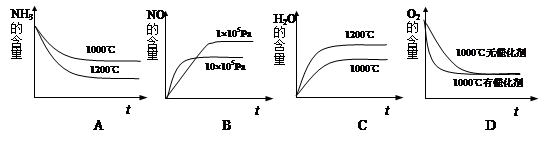
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 C(g) △H<0。达到平衡时,C的体积分数为40%。试回答有关问题:
C(g) △H<0。达到平衡时,C的体积分数为40%。试回答有关问题:| A.一定向正反应方向移动 | B.一定向逆反应方向移动 |
| C.一定不移动 | D.不一定移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3,下列判断正确的是
2SO3,下列判断正确的是 | A.2体积SO2和足量O2反应,必定生成2体积SO3 |
| B.其他条件不变,增大压强,平衡必定向右移动 |
| C.平衡时SO2消耗速度必定等于O2生成的速度 |
| D.平衡时SO2浓度必定等于O2浓度的两倍 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g)+H2(g) , 试分析和回答下列问题:
CO(g)+H2(g) , 试分析和回答下列问题:| A.体系的压强不再发生变化 |
| B.v正(CO)=v逆(H2O) |
| C.生成n mol CO的同时生成n mol H2 |
| D.1 mol H-H键断裂的同时断裂2 mol H-O键 |
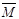 的取值范围是 。
的取值范围是 。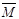 1),分别给出
1),分别给出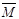 的变化:(填“增大”、“减小”、“不变”)
的变化:(填“增大”、“减小”、“不变”)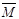 1的取值 1的取值 | 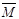 的变化 的变化 |
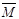 1<12 1<12 | |
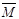 1=12 1=12 | 不变 |
 1>12 1>12 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) △H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表。下列叙述正确的是
2NH3(g) △H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表。下列叙述正确的是| 容器 编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com