
【题目】PbCrO4是一种黄色颜料,制备PbCrO4的一种实验步骤如图1:

已知:①Cr(OH)3(两性氢氧化物)呈绿色且难溶于水
②Pb(NO3)2、Pb(CH3COO)2均易溶于水,PbCrO4的Ksp为2.8×10﹣13,Pb(OH)2开始沉淀时pH为7.2,完全沉淀时pH为8.7。
③六价铬在溶液中物种分布分数与pH关系如图2所示。

④PbCrO4可由沸腾的铬酸盐溶液与铅盐溶液作用制得,含PbCrO4晶种时更易生成
(1)实验时需要配置100mL3molL﹣1CrCl3溶液,现有量筒、玻璃棒、烧杯,还需要玻璃仪器是___。
(2)“制NaCrO2(aq)”时,控制NaOH溶液加入量的操作方法是_____。
(3)“氧化”时H2O2滴加速度不宜过快,其原因是_____;“氧化”时发生反应的离子方程式为___。
(4)“煮沸”的目的是_____。
(5)请设计用“冷却液”制备PbCrO4的实验操作:_____[实验中须使用的试剂有:6molL﹣1的醋酸,0.5molL﹣1Pb(NO3)2溶液,pH 试纸]。
【答案】100 mL容量瓶和胶头滴管 不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解 减小H2O2自身分解损失 2CrO2- +3H2O2 +2OH-===2CrO![]() +4H2O 除去过量的H2O2 ①在不断搅拌下,向“冷却液”中加入6 mol·L-1的醋酸至弱酸性,用pH试纸测定略小于,②先加入一滴0.5 mol·L-1 Pb(NO3)2溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,静置,③向上层清液中滴入Pb(NO3)2溶液,④若无沉淀生成,停止滴加Pb(NO3)2溶液,静置、过滤、洗涤、干燥沉淀得PbCrO4
+4H2O 除去过量的H2O2 ①在不断搅拌下,向“冷却液”中加入6 mol·L-1的醋酸至弱酸性,用pH试纸测定略小于,②先加入一滴0.5 mol·L-1 Pb(NO3)2溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,静置,③向上层清液中滴入Pb(NO3)2溶液,④若无沉淀生成,停止滴加Pb(NO3)2溶液,静置、过滤、洗涤、干燥沉淀得PbCrO4
【解析】
Cr(OH)3为两性氢氧化物,在CrCl3溶液中滴加NaOH溶液可生成NaCrO2,“制NaCrO2(aq)”时,控制NaOH溶液加入量,应再不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解,再加入6%H2O2溶液,发生氧化还原反应生成Na2CrO4, “氧化”时H2O2滴加速度不宜过快,可减小H2O2自身分解损失,经煮沸可除去H2O2,冷却后与铅盐溶液作用制得PbCrO4,以此解答该题。
(1)实验时需要配置100mL3molL﹣1CrCl3溶液,现有量筒、玻璃棒、烧杯,还需要玻璃仪器是100mL容量瓶和胶头滴管,其中胶头滴管用于定容,故答案为:100mL容量瓶和胶头滴管;
(2)Cr(OH)3为两性氢氧化物,呈绿色且难溶于水,加入氢氧化钠溶液时,不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解,可防止NaOH溶液过量,故答案为:不断搅拌下逐滴加入NaOH溶液,至产生的绿色沉淀恰好溶解;
(3)“氧化”时H2O2滴加速度不宜过快,可防止反应放出热量,温度过高而导致过氧化氢分解而损失,反应的离子方程式为2CrO2﹣+3H2O2+2OH﹣=2CrO42﹣+4H2O,故答案为:减小H2O2自身分解损失;2CrO2﹣+3H2O2+2OH﹣=2CrO42﹣+4H2O;
(4)煮沸可促使过氧化氢分解,以达到除去过氧化氢的目的,故答案为:除去过量的H2O2;
(5)“冷却液”的主要成分为Na2CrO4,要想制备PbCrO4,根据已知信息②由Pb(NO3)2提供Pb2+,但要控制溶液的pH不大于7.2,以防止生成Pb(OH)2沉淀,由信息③的图象可知,溶液的pH又不能小于6.5,因为pH小于6.5时CrO42﹣的含量少,HCrO4﹣的含量大,所以控制溶液的pH略小于7即可,结合信息④,需要先生成少许的PbCrO4沉淀,再大量生成。所以实验操作为在不断搅拌下,向“冷却液”中加入6molL﹣1的醋酸至弱酸性(pH略小于7),将溶液加热至沸腾,先加入一滴0.5 molL﹣1Pb(NO3)2溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,静置,向上层清液中滴入Pb(NO3)2溶液,若无沉淀生成,停止滴加,静置、过滤、洗涤、干燥;
故答案为:①在不断搅拌下,向“冷却液”中加入6 mol·L-1的醋酸至弱酸性,用pH试纸测定略小于,②先加入一滴0.5 mol·L-1 Pb(NO3)2溶液搅拌片刻产生少量沉淀,然后继续滴加至有大量沉淀,静置,③向上层清液中滴入Pb(NO3)2溶液,④若无沉淀生成,停止滴加Pb(NO3)2溶液,静置、过滤、洗涤、干燥沉淀得PbCrO4。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
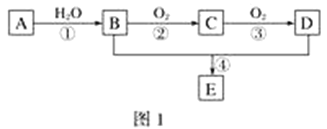
(1)写出下列物质的官能团名称:B:____________________;D:____________________。
(2)反应④的化学方程式为________________________________________________,反应类型:________。
(3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。
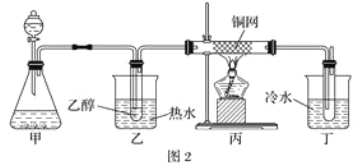
①装置甲锥形瓶中盛放的固体药品可能为________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_______________________________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
![]()
(1)该小组同学欲用图所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。

① 应该选择的仪器是__________(填字母)。
② 将各仪器按先后顺序连接起来,应该是a接__________,__________接__________,__________接__________,__________接h(用导管口处的字母表示)。
③ 浓盐酸与二氧化锰反应的离子方程式为__________。
(2)该小组同学设计分别利用图所示装置探究氯气的氧化性。
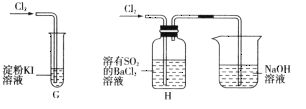
①G中的现象是__________,原因是__________(用化学方程式表示)。
②H中的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,根据下图所示的关系:

(1)确定A、B、C、D、E、F的化学式,A为________,B为________,C为________,D为________,E为________,F为________。
(2)写出⑧的化学方程式,④、⑤的离子方程式。
⑧_________________________________________________,
④________________________________________________,
⑤___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】慢心律是一种治疗心律失常的药物。它的合成路线如图所示。
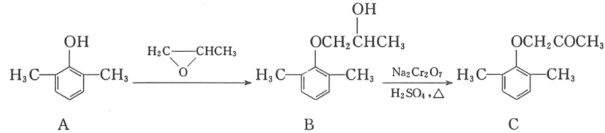
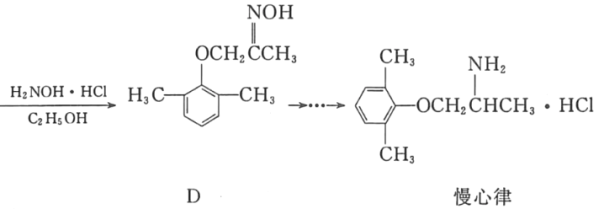
(1)C中的含氧官能团名称为_____和_____;
(2)由B→C的反应类型是_____。
(3)由A制备B的过程中有少量副产物E,它与B互为同分异构体。写出E的结构简式:_____。
(4)写出同时满足下列条件的化合物D的一种同分异构体的结构简式:_____。
①属于a﹣氨基酸;②是苯的衍生物,且苯环上的一氯代物只有两种;③分子中有2个手性碳原子
(5)已知乙烯在催化剂作用下与氧气反应可以生成环氧乙烷(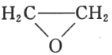 )。写出以邻甲基苯酚(
)。写出以邻甲基苯酚( )和乙醇为原料制备
)和乙醇为原料制备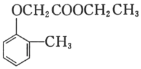 的合成路线流程图(无机试剂任用)。合成路线流程图示例见本题题干_____。
的合成路线流程图(无机试剂任用)。合成路线流程图示例见本题题干_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 当H2O与Na2O2反应生成1molO2时,转移的电子数目为2×6.02×1023
B. 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C. 常温下2S2O(g)![]() 3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应
3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应
D. 氯水通入SO2后溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是元素周期表中的短周期元素,它们的相对位置如下表所示,其中X、Y 元素均能形成10电子的氢化物,Z的原子序数是Y的2倍。请回答下列问题:
X | Y | |
Z | W |
(1)W的简单离子的结构示意图为______,Y元素在周期表中的位置是____。
(2)写出实验室制W元素单质的离子方程式:___________
(3)关于W同主族元素,下列说法正确的是:__________
A.从上到下密度逐渐增大
B.从上到下熔点和沸点都逐渐升高
C.从上到下元素的非金属性越来越强
D.同主族元素对应的单质中,只有W元素对应的单质在常态下为气态
(4)W与Z形成的液体化合物Z2W2,该物质可与水反应生成ZO2气体,1 mol Z2W2参加反应时转移1.5 mol电子,其中只有一种元素化合价发生改变,Z2W2与水反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)根据如图提供的信息,写出该反应的热化学方程式___,如图的曲线中__(填“a”或“b”)表示加入铁触媒(催化剂)的能量变化曲线。

(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是___。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成nmolN2的同时生成2nmolNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)500℃、50MPa时,在容积为1L的容器中加入1molN2、3molH2,反应达平衡后测得平衡常数为K,此时N2的转化率为a。则K和a的关系是K=___。
(4)1998年希腊亚里斯多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电解合成氨。其实验装置如图。阴极的电极反应式为___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
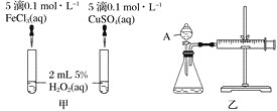
(1)若利用图甲装置,可通过观察__________现象,从而定性比较得出结论。
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是 ________。写出H2O2在二氧化锰催化作用下发生反应的化学方程式:___________。
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为________,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是________。
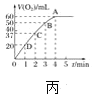
(4)将0.1molMnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:________。H2O2初始物质的量浓度为_______(保留两位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com