
Na2SO4(s)+4H2(g)![]() Na2S(s)+4H2O(g);ΔH>0
Na2S(s)+4H2O(g);ΔH>0
若反应在恒温恒容状态下进行,回答以下问题:
(1)向容器中分别加入以下物质,判断对平衡有无影响,有影响的应填写出平衡移动的方向。
①加入Na2SO4__________________________________________。
②加入焦炭_____________________________________________。
(2)若将容器温度升高20 ℃,H2在混合气体中的含量变化用下图中______图表示最合适。
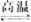
(1)①无影响 ②有影响,正向移动 (2)D
解析:(1)对于已处于化学平衡状态的体系,固体反应物的量对平衡无影响,故加入Na2SO4固体时平衡不移动。但加入固体焦炭时,由于体系温度为1000 ℃,会发生如下反应:
C+H2O(g)![]() CO+H2
CO+H2
使原平衡体系中的c(H2O)减小,c(H2)增大,平衡向右移动。
(2)若升高温度,由于原平衡的反应为吸热反应,故平衡向正反应方向移动,φ(H2)的含量应逐渐减少,直至达到新的平衡。分析A、B、C、D的曲线走向,唯D项正确。
常见错解:因未意识到1000 ℃时焦炭与水蒸气的反应,而仅仅认为焦炭是与该反应无关的固体,从而得出焦炭的加入对原平衡无影响的错误结论。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是____________________________。
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)![]() 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将___________。(填““增大”“减小”或“不变”)
②下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1 000 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为__________。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2___________T1。
(3)下图所示装置可用于制备N2O5,则N2O5在电解池的_______区生成,其电极反应式为____________________________________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
N2O5—是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 (填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为 。
③在T3温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1。
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的 区生成,其电极反应式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
N2O5是一种新型硝化剂,其性质和制备受到人们的关注。![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)一定温度下,在恒容密闭容器中N2 O5可发生下列反应:
![]() 2N2O5(g) 4NO2(g)+O2(g);ΔH>0
2N2O5(g) 4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 。(填“增大”或“减小”、“不变”)
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500s内N2O5的分解速率为 。
③在T3温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1。
 |
(3)如上图所示装置可用于制备N2O5,则N2O5在电解池的
区生成,其电极反应式为 .
查看答案和解析>>
科目:高中化学 来源:2008年普通高等学校招生统一考试理综试题化学部分(重庆卷) 题型:填空题
N2O5—是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 (填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化学 来源:2015届山东省高二上学期期中考试化学试卷(解析版) 题型:选择题
在1 000 K时,已知反应Ni(s)+H2O(g)  NiO(s)+H2(g)的平衡常数K=0.059,当水蒸气和氢气的物质的量浓度相等时,此反应
NiO(s)+H2(g)的平衡常数K=0.059,当水蒸气和氢气的物质的量浓度相等时,此反应
A.已达平衡状态 B.未达平衡状态,反应正向进行
C.未达平衡状态,反应逆向进行 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com