
在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol?L-1和1.5 mol?L-1,现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是
A.反应后溶液中Fe3+物质的量为0.8 mol
B.反应后产生13.44 L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol
D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体
C
【解析】
试题分析:1 L溶液中含有Fe(NO3)3和H2SO4两种溶质的物质的量分别是0.2mol、1.5mol,则n(H+)=3.0mol,n(NO3-)=0.2mol×3=0.6mol,n(Fe)=39.2g/56g/mol=0.7mol,首先发生Fe+NO3-+4H+=3Fe3++NO↑+2 H2O,根据所给数据可知0.6mol NO3-需要0.6molFe、2.4molH+,所以生成0.6mol Fe3+,原溶液中有0.2mol Fe3+,则此时溶液中共有0.8mol Fe3+,所以过量3.0-2.4=0.6mol的H+和0.1molFe,根据氧化性Fe3+>H+,可知剩余的Fe与Fe3+反应, Fe+2 Fe3+=2Fe2+,所以0.1molFe与0.2mol铁离子反应生成0.3mol Fe2+,此时溶液中存在0.3mol Fe2+和0.6mol Fe3+,二者物质的量之和是0.9mol。A、反应后溶液中铁离子的物质的量是0.6mol,错误;B、该反应过程中无氢气生成,错误;C、反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol,正确;D、反应开始有气体生成为NO气体,后无气体生成,错误,答案选C。
考点:考查铁与混酸的反应,离子方程式在计算中的应用


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.0.1 mol·L-1Na2S溶液中含有的Na+离子数为0.2NA
B.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
C.标准状况下,22.4 L以任意比例混合的氢气和氯气混合气中含有的原子总数为2NA
D.0.10 mol Fe粉与足量水蒸气反应生成的H2分子数为0.10NA
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第二次检测考试化学试卷(解析版) 题型:选择题
下列实验操作完全正确的是
编号 | 实验 | 操作 |
A | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容 |
C | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接受容器,上层液体继续从分液漏斗下端管口放出 |
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三第一次联考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列叙述正确的是
A.78gNa2O2固体中含有的阴离子数为NA
B.标准状况下,2.24L氖气所含原子数为0.2NA
C.1L 0.1 mol/L醋酸溶液中含有的氢离子数为0.1NA
D.标准状况下,2.24L己烷含有分子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三第一次诊断考试化学试卷(解析版) 题型:填空题
(10分)在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中的若干种离子:
阳离子 | K+、Ag+、Mg2+、Ba2+ |
阴离子 | NO3-、CO32-、SiO32-、SO42- |
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
Ⅲ | 在Ⅱ的滤液中滴加BaC12溶液 | 无明显现象 |
试回答下列问题:
(1)实验I能确定一定不存在的阳离子是 。
(2)实验I中生成沉淀的离子方程式为 。
(3)通过实验I、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
阴离子 | NO3- | CO32- | SiO32- | SO42- |
c/mol·L-1 |
|
|
|
|
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由 。
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三第一次诊断考试化学试卷(解析版) 题型:选择题
下列叙述中正确的个数是
①有新单质生成的化学反应一定是氧化还原反应。
②熵增且放热的反应一定是自发反应。
③Mg比A1活泼,在Mg和A1形成的原电池中,Mg必定做负极。
④难溶电解质的溶度积越小,则它的溶解度越小。
⑤燃烧热是指1 mol可燃物完全燃烧生成氧化物时所释放的能量。
⑥干燥的C12和氯水均能使鲜花褪色
A.1 B.2 C.3 D.4
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三第一次诊断考试化学试卷(解析版) 题型:选择题
下列相关反应的离子方程式书写正确的是
A.氢氧化铁溶于氢碘酸:Fe(OH)3 +3H+ =Fe3++3H2O
B.向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2=2Fe3+ +2Cl-
C.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3—+Ba2++2OH— = BaCO3? +2H2O+CO32—
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高一上学期期中考试化学试卷(解析版) 题型:选择题
同温同压时,等质量的下列气体所占有的体积最大的是
A.O2 B.CH4 C.CO2 D.H2
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(理)试卷(解析版) 题型:填空题
(17分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g)  2NH3(g) △H= -92.4 kJ/mol,据此回答以下问题:
2NH3(g) △H= -92.4 kJ/mol,据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是 (填序号)。
①反应压强为20Mpa~50Mpa
②500℃的高温
③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中。
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),
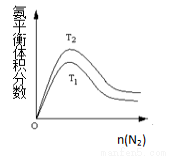
判断的依据是: 。(3分)
(3)合成氨气所需的氢气可以由水煤气分离得到。
涉及反应信息如下:
反应一:C(s)+H2O(g)  H2(g)+CO(g) 平衡常数K1
H2(g)+CO(g) 平衡常数K1
反应二:CO(g)+H2O(g)  H2(g)+CO2(g) 平衡常数K2
H2(g)+CO2(g) 平衡常数K2
① K1的表达式:K1= 。(3分)
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
实验组别 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
3 | T | a | b | c | d | t |
(Ⅰ)实验1中,用CO2表示反应开始到平衡的平均反应速率为 。
(Ⅱ)在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为 (填序号)(3分)
A.其它条件不变温度T<900℃ B.其它条件不变温度T>900℃
C.充入一定量氖气 D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com