
����Ŀ��CH3OH ��һ����ɫ�д̼�����ζ��Һ�壬����������������Ҫ��;��
��.Ŀǰ��ҵ����һ�ַ������� CO2 ����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g) +3H2(g)=CH3OH(g)+H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��
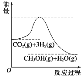
(1)����Ϊ�÷�ӦΪ_____(����Ȼ�����)��Ӧ.
(2)���������У��������Ϸ�Ӧ���ܼӿ췴Ӧ���ʵ���_____��
a�������¶� b������ He c��������� d������ѹǿ
��. CH3OH Ҳ��һ����Ҫ��ȼ�ϣ�һ�������·�����Ӧ��
2CH3OH(g)��3O2(g) =2 CO2(g)��4H2O(g)��
(3)ij�¶��£��� 4mol CH3OH �� 6 mol O2 ���� 2 L ���ܱ������о��� 4 min ��Ӧ�ﵽƽ�⣬��� c(O2)��1.5mol��L��1��4 min ��ƽ����Ӧ���� ��(H2O)��_____��
(4)CH3OH ȼ�ϵ����Ŀǰ������ɹ���ȼ�ϵ��֮һ������ȼ�ϵ���ɼ״�������(����)��KOH(�������Һ)���ɡ�������˵����ȷ����_____(�����)��
�ٵ�طŵ�ʱͨ������ĵ缫Ϊ����
�ڵ�طŵ�ʱ���������Һ�ļ�������
�۵�طŵ�ʱÿ���� 6.4 g CH3OH ת�� 1.2 mol ����
(5)�� CH3OH������(����)������������ҺΪԭ�ϣ�ʯīΪ�缫����ȼ�ϵ�أ��õ���и����ϵĵ缫��Ӧʽ�ǣ�____________________________��
���𰸡����� ac 0.5mol��(L��min)-1 �ڢ� CH3OH+8OH--6e-=CO32-+6H2O
��������
��.(1)��Ϸ�Ӧ������������������С�Ƚ��жϷ�Ӧ���Ȼ����ȣ�
(2)���ݸı���������Ի�ѧ��Ӧ���ʵ�Ӱ����з������
��.(3)���ݹ�ʽ![]() ����O2�Ļ�ѧ��Ӧ���ʣ��ٽ�ϻ�ѧ�������뻯ѧ��Ӧ���ʳ����ȼ���H2O�Ļ�ѧ��Ӧ���ʣ�
����O2�Ļ�ѧ��Ӧ���ʣ��ٽ�ϻ�ѧ�������뻯ѧ��Ӧ���ʳ����ȼ���H2O�Ļ�ѧ��Ӧ���ʣ�
(4)��(5)CH3OHȼ�ϵ���У�KOH���������Һ��CH3OH��������ʧȥ���ӷ���������Ӧ���缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��O2���������õ����ӷ�����ԭ��Ӧ���缫��ӦʽΪO2+4e-+2H2O=4OH-���ݴ˷������
��. (1)����ͼ���֪����Ӧ������������������������������˸÷�ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
(2)���������У����ڷ�ӦCO2(g) +3H2(g)=CH3OH(g)+H2O(g)��
a�������¶ȣ���ѧ��Ӧ���ʼӿ죬a�������⣻
b�����������³���He�������ʵ�Ũ�Ȳ��䣬��ѧ��Ӧ���ʲ������ı䣬b���������⣻
c����������ɽ��ͷ�Ӧ�Ļ�ܣ���ѧ��Ӧ���ʼӿ죬c�������⣻
d������ѹǿ��ѧ��Ӧ���ʼ�����d���������⣻
�ʴ�Ϊ��ac��
��.(3)��4min��O2ת�������ʵ���Ϊxmol������6mol-xmol=1.5mol/L��2L��x=3���� ���ɻ�ѧ��Ӧ�����뻯ѧ�����������ȿɵ���(O2)����(H2O)=3��4������(H2O)=
���ɻ�ѧ��Ӧ�����뻯ѧ�����������ȿɵ���(O2)����(H2O)=3��4������(H2O)=![]() ��(O2)=
��(O2)=![]() ��0.375mol��L-1��min-1=0.5 mol��L-1��min-1���ʴ�Ϊ��0.5mol��L-1��min-1��
��0.375mol��L-1��min-1=0.5 mol��L-1��min-1���ʴ�Ϊ��0.5mol��L-1��min-1��
(4)�ٸ�������������֪����طŵ�ʱ��O2����������ͨ������ĵ缫Ϊ�������ٴ���
�ڵ�طŵ�ʱ����ص��ܷ�ӦΪ2CH3OH+3O2+4OH-=2CO32-+6H2O���������Һ��OH-���ϱ����ģ���������������ȷ��
�۵�طŵ�ʱ��������ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O��6.4gCH3OH��������Ϊ6.4g��32g/mol=0.2mol��ÿ����0.2molCH3OHת��0.2mol��6=1.2mol���ӣ�����ȷ��
�ʴ�Ϊ���ڢۣ�
(5)��������������֪��CH3OHȼ�ϵ���У�KOH���������Һ��CH3OH��������ʧȥ���ӷ���������Ӧ���缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O���ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ�ϵ��Ϊ��Դ���е���ʵ��װ��ʾ��ͼ��ͼ��ʾ������˵����ȷ������ ��
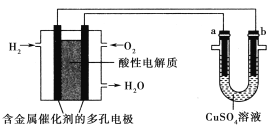
A��ȼ�ϵ�ع���ʱ��������ӦΪO2��2H2O��4e��=4OH��
B����װ�������������ͭʱ��aΪ��bΪCu������һ��ʱ��Ҫʹ�ҳ���Һ��ԭ�ɼ���������CuO
C��a���Ǵ�ͭ��b���Ǵ�ͭʱ��a�����ܽ⣬b������ͭ����
D����a��b������Ϊʯīʱ������ͬ�����£�a���������������������ĵ�H2�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊһ�����ʹ��ܵ�أ���Ӧ���õ����Ӻͷ�չ�������������ڽ����ơ�������Ͷ�������Na2SX���ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մ����ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ1��ʾ��
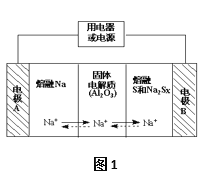

��1�����ݱ����ݣ������жϸõ�ع���������Ӧ����
��_____������ĸ����Χ����
A��100������ B��100��300��
C��300��350�� D��350��2050��
���� | Na | S | Al2O3 |
�۵�/�� | 97.8 | 115 | 2050 |
�е�/�� | 892 | 444.6 | 2980 |
��2���ŵ�ʱ���缫AΪ_____�����缫B����_____��Ӧ������������ԭ������
��3�����ʱ���ܷ�ӦΪNa2Sx��2Na+xS���������ĵ缫��ӦʽΪ��________________��
��4��������������Ϊ��Դ��������װ��KI��������Һ��ͼ2��ʾ�����ڵ��м��������ӽ���Ĥ������ͨ��һ��ʱ����������Һ����ɫ��һ��ʱ�����ɫ��dz�����Ҳ���ĵ缫����ʽ��________________���Է��������Һ��ɫ��dz�Ŀ���ԭ���ǣ�___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���2��1��ϩ[CH2=C(CH3)CH2CH3]��˵��������ǣ� ��
A. ��1-��ϩ(CH2=CHCH2CH3)��Ϊͬϵ��
B. �������м���̼̼˫��
C. ���л��������̼ԭ�ӿ��ܹ�ƽ��
D. �뻷����(![]() )��Ϊͬ���칹��
)��Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(1)��״���£�1.7 g NH3��_______L H2S���庬�е���ԭ������ͬ��
(2)2 mol��CO2��3 mol��SO3��ԭ����֮����__________��
(3)���³�ѹ��22.4��CO2�з��Ӹ���___64��SO2�ķ��Ӹ���(��������������)
(4)��״���£�33.6L��NH3�������ӵ����ʵ���ԼΪ______mol�������ܽ���ˮ���1L����Һ������Һ�����ʵ���Ũ��Ϊ__________mol/L
(5)��һ���¶Ⱥ�ѹǿ�£�0.4molij��������Ϊ9.8L����������µ�����Ħ�����Ϊ________��
(6)ij�λ����Һ�к������ӣ�Na+��Mg2+��Cl����SO42�������Na+��Mg2+ ��Cl�������ʵ���Ũ������Ϊ��0.2molL��1��0.25molL��1��0.4molL��1����c(SO42��)=__________��
(7)�е������NaCl��CaCl2��AlCl3������Һ���ֱ���������AgNO3��Һ��Ӧ�������ɳ�����������ȣ���������Һ���������ʵ����ʵ���Ũ��֮��Ϊ_____________��
(8)��״���£�NH3��CH4��ɵĻ�������ƽ���ܶ�Ϊ0.75g/L���û�������ƽ��Ħ������Ϊ_________________��NH3���������Ϊ______________.
(9)VmLAl2(SO4)3��Һ�к�Al3+ ag��ȡ0.5VmL��Һϡ�͵�2VmL����ϡ�ͺ���Һ��SO42�������ʵ���Ũ����_____________mol/L��
���밴��Ҫ��������з���ʽ��
(1)д����ĭ�������Ӧԭ�������ӷ���ʽ��_______________________________________��
(2)����ˮ���������·�Ӧ�Ļ�ѧ����ʽ��____________________________________________��
(3)NaCN���ھ綾���ʣ���һ�ִ���������ԭ��ΪCN����S2O32-��Ӧ�����������ӣ�һ����Fe3�������ɺ�ɫ��Һ����һ����H�����ò�����ʹƷ����Һ��ɫ�Ĵ̼������壬д��CN����S2O32-��Ӧ�����ӷ���ʽ��___________________________________��
(4)���������Ƕ��Խ�ǿ�����ʣ�����н�ǿ�Ļ�ԭ�ԣ�������������Һ�μӵ�K2Cr2O7������Һ(��ɫ)�У���Һ�ɳ�ɫ��Ϊ��ɫ(Cr3��)����д����Ӧ�����ӷ���ʽ��__________________________��
(5)��NaHSO4��Һ��������������Һ�������Ե����ӷ�Ӧ����ʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����0.100 mol��L��1��NaOH��Һ�ζ�20.00 mL 0.100 mol��L��1��HNO2��Һ��![]() ������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��

A. 25 ��ʱ��0.100 mol��L��1��HNO2��Һ��pH��2.75
B. B���Ӧ����Һ�У�2c(H��)��c(HNO2)��c(NO2-)��2c(OH��)
C. C���Ӧ����Һ��pH��7������NaOH��Һ�����Ϊ20.00 mL
D. �ζ������д�A��D����Һ��ˮ�ĵ���̶���������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п�̵�����ճ����������������ĵ�أ��乹����ͼ��ʾ���ŵ�ʱ�ܷ�ӦΪ��Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH��
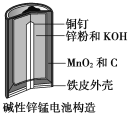
�ӷϾɼ���п�̵���л���Zn��MnO2�Ĺ�����ͼ��ʾ��
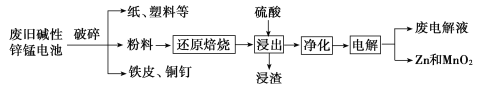
�ش��������⣺
(1)MnOOH�У�MnԪ�صĻ��ϼ�Ϊ_________��
(2)����ԭ�����������У��۽��������ﱻ��ԭΪ�ͼ���������������(����MnOOH��MnO2����ԭ��MnO)����Ҫԭ�������������к���_________��
(3)����������Ϊ�˳�ȥ����Һ�е�Fe2���������ǣ�����______(�ѧʽ)��Һ��Fe2������ΪFe3�����ٵ���pHʹFe3��������ȫ�������£���֪����Һ��Mn2����Zn2����Ũ��ԼΪ0.1 mol/L�������������ݼ��㣬����pH�ĺ�����Χ��______��__________��(����Ũ��С��1��10��5 mol/L��Ϊ������ȫ)
������ | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
Ksp����ֵ | 10��13 | 10��17 | 10��38 |
(4)�������ʱ�������ĵ缫��ӦʽΪ_________����������Ӧѭ�����õ�������_______(�ѧʽ)��
(5)������������ֱ�������Ṳ�ȷ�Ӧ����ˣ���Һ����Ҫ�ɷ���ZnCl2��MnCl2��������һ�ֻ���ɫ���壬���������е�MnOOH�����ᷴӦ�Ļ�ѧ����ʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����Ҫ�Ļ����м��壬������ҵ�о����ȵ㡣һ����ʯ�ͻ����еķ�������(��Ҫ�ɷ�ΪNiCO3��SiO2������������Fe2O3��Cr2O3)Ϊԭ���Ʊ��������Ĺ�ҵ������ͼ��
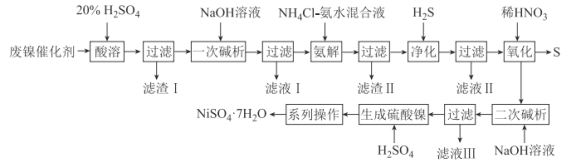
��֪����NiS��Ni(OH)2��Cr(OH)3��������ˮ��Cr(OH)3�������������
��Fe(OH)3������NH4Cl-��ˮ�Ļ��Һ��Ni(OH)2����NH4Cl��ˮ�Ļ��Һ����[Ni(NH3)6]2+��
��ش��������⣺
(1)��������ʱΪ�ӿ췴Ӧ���ʣ������Ԫ�صĽ����ʣ����Բ�ȡ�Ĵ�ʩ�У�________��
(2)��������������Ҫ�ɷ�Ϊ__���ѧʽ�����������ڹ�ҵ�ϵ���;Ϊ_________����дһ�֣���
(3)��һ�μ�����ʱ�������NaOH��Һ���������Ŀ����_________��
(4)��������������Ӧ�����ӷ���ʽΪ________����������ʱͨ��H2S��Ŀ����_______��
(5)��������ʱ������Ӧ�Ļ�ѧ����ʽΪ_________��
(6)��ϵ�в�����������ָ_________�����ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����120����101kPa�£�a mL����������ϩ��ɵĻ��������b mL�����г��ȼ�պָ���ԭ�¶Ⱥ�ѹǿ����֪b > 3a����ȼ�պ����������С��b/16mL������ϩ�����Ϊ�� ��
A��b/16mL ��������B��b/8mL ���������� C��(a- b/8) mL ������D��(a+ b/8) mL
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com