
| A. | 0.1mol/L的NaHA其PH=1,溶液中存在:c(Na+)+c(H+)=c(OH-)+2c(A2-)+c(HA-) | |
| B. | 40%的醋酸溶液(p=1.049gcm-3)与60%的醋酸溶液(p=1.064gcm-3)等体积混合后,所得溶液中溶质的质量分数大于50% | |
| C. | 0.1mol/L的醋酸溶液V1L和等浓度的氢氧化钠溶液V2L混合后呈碱性,则一定有V1≤V2 | |
| D. | 1L0.5mol/LFeCl3的溶液与0.2L1mol/LKCl溶液中Cl-数目之比为15:2 |
分析 A.溶液中存在电荷守恒,阴阳离子所带电荷总数相同;
B.设体积为1ml,计算40%醋酸溶液和60%的醋酸溶液中溶质质量,溶液质量m=ρV,结合溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
C.0.1mol/L的醋酸溶液V1L和等浓度的氢氧化钠溶液V2L混合后呈碱性,c(H+)<c(OH-),电荷守恒分析;
D.根据溶液的浓度和化合物的组成判断两种溶液中离子浓度的关系,注意与溶液的体积无关,然后求出离子的物质的量,利用数目之比等于物质的量之比.
解答 解:A.0.1mol/L的NaHA其PH=1,说明NaHA完全电离,溶液中无HA-离子,溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+2c(A2-),故A错误;
B.40%的醋酸溶液(p=1.049gcm-3)与60%的醋酸溶液(p=1.064gcm-3)等体积混合后,设体积为1ml,混合后溶质质量分数=$\frac{40%×1.049g/ml×1ml+60%×1.064g/ml×1ml}{1.049g/ml×1ml+1.064g/ml×1ml}$×100%=50.1%,故B正确;
C.0.1mol/L的醋酸溶液V1L和等浓度的氢氧化钠溶液V2L混合后呈碱性,c(H+)<c(OH-),电荷守恒为:c(H+)+c(Na+)=c(OH-)+c(CH3COO-),只需满足c(Na+)>c(CH3COO-),当V1>V2时也可以溶液显碱性,故C错误;
D.1L0.5mol/LFeCl3的溶液c(Cl-)=3c(FeCl3)=3×0.5mol/L=1.5mol/L,n(Cl-)=1L×1.5mol/L=1.5mol;0.2L 1mol/L KCl溶液中c(Cl-)=c(KCl)=1mol/L,n(Cl-)=0.2L×1mol/L=0.2mol,所以数目之比等于1.5mol:0.2mol=15:2,故D正确;
故选BD.
点评 本题考查了盐类水解、溶质质量分数计算、离子浓度计算、电解质溶液中电荷守恒,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 1:2:6 | B. | 2:1:6 | C. | 8:8:117 | D. | 117:4:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用两只250 mL的容量瓶配制0.1 mol/L 500 mL的NaOH溶液 | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28 mL | |
| C. | 常温常压下测得1 mol N2的质量为28 g | |
| D. | 用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①或② | B. | ②或④ | C. | ①或③ | D. | ③或④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | X试剂 | 离子方程式 |
| A | Fe2+、Na+、SO42-、Cl- | 碘水 | 2Fe2++I2═2Fe3++2I- |
| B | pH=8的溶液中:Na+、HCO3-、Cl- | 少量澄清石灰水 | Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- |
| C | 透明溶液中:NH4+、Fe3+、Cl-、AlO2- | 过量铜粉 | Cu+2Fe═2Fe2++Cu2+ |
| D | K+、Na+、SO42-、ClO- | 少量SO2 | 2Cl-+SO2+H2O═2HClO+SO32- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(Y)>r(Z)>r(W) | |
| B. | 元素Z、W的简单离子的电子层结构相同 | |
| C. | 元素Y 的简单气态氢化物的热稳定性比Z 的强 | |
| D. | 只含X、Y、Z三种元素的化合物,一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
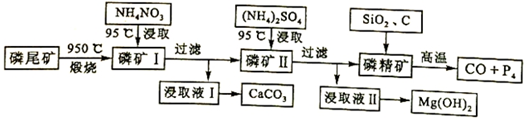
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
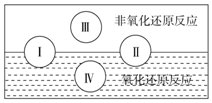 氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
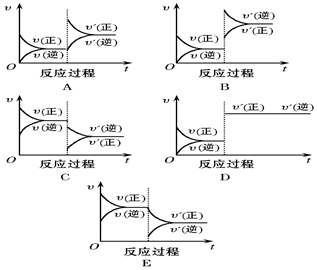 在一定条件下,反应A(g)+2B(s)?C(g)(正反应为吸热反应)达到平衡后,根据下列图象判断:
在一定条件下,反应A(g)+2B(s)?C(g)(正反应为吸热反应)达到平衡后,根据下列图象判断:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com