
【题目】碱性电池具有容量大、放电电流大的特点因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解质溶液,电池总反应式为:Zn+2MnO2+H2O=Zn(OH)2+Mn2O3。下列说法正确的是( )
A.电池工作时,锌是正极
B.电子由Zn电极通过外电路流向MnO2电极
C. MnO2电极发生氧化反应
D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5 g
【答案】B
【解析】
A.根据电池反应:Zn+2MnO2+H2O=Zn(OH)2+Mn2O3可知:金属锌失电子,发生氧化反应,作负极,A错误;
B.金属锌作负极,失电子,发生氧化反应;MnO2作正极,得电子,发生还原反应,电子从负极Zn流向正极MnO2,B正确;
C.MnO2得电子发生还原反应,C错误;
D.由Zn+2MnO2+H2O=Zn(OH)2+Mn2O3可知:1 mol Zn反应失去2 mol电子,则转移0.1 mol电子,需要Zn的物质的量是n(Zn)=![]() ×0.1 mol=0.05 mol,其质量m(Zn)=0.05 mol×65 g/mol=3.25 g,D错误;
×0.1 mol=0.05 mol,其质量m(Zn)=0.05 mol×65 g/mol=3.25 g,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】溴化亚铜是一种白色粉末,不溶于冷水,在热水中或见光都会分解,在空气中会慢慢被氧化。实验室制备![]() 的步骤如下:
的步骤如下:
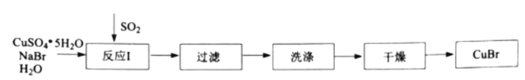
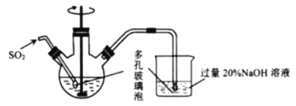
(1)反应Ⅰ在如图所示实验装置的三颈烧瓶中进行,实验所用蒸馏水需经煮沸,目的是除去水中的_________(写化学式)。
(2)反应Ⅰ中:三颈烧瓶中反应生成![]() 的离子方程式为________;烧杯中发生反应的化学方程式为________。
的离子方程式为________;烧杯中发生反应的化学方程式为________。
(3)过滤步骤中,需要在避光的条件下进行,原因是________。
(4)洗涤步骤中,依次用溶有少量![]() 的水、溶有少量
的水、溶有少量![]() 的乙醇、纯乙醚洗涤。洗涤剂需“溶有
的乙醇、纯乙醚洗涤。洗涤剂需“溶有![]() ”的原因是________。
”的原因是________。
(5)欲利用上述装置烧杯中的吸收液制取较纯净的无水![]() 晶体。
晶体。
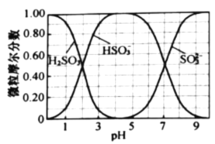
(水溶液中![]() 、
、![]() 、
、![]() 随
随![]() 的分布,
的分布,![]() 的溶解度曲线如题图所示)。
的溶解度曲线如题图所示)。
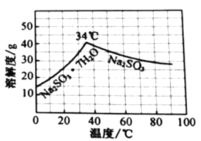
请补充完整实验方案[须用到![]() (贮存在钢瓶中)、
(贮存在钢瓶中)、![]() 计]:
计]:
①________;
②加入少量维生素C溶液(抗氧剂),加热浓缩溶液至有大量晶体析出;
③________;
④用无水乙醇洗涤2-3次;
⑤放真空干燥箱中干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去),下列推断不正确的是
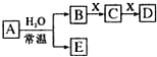
A.若X是Na2CO3,C为CO2,则A一定是氯气,此时D和E不反应
B.若X是CO2,B和D的反应是OH-+![]() =
=![]() +H2O,则E一定能还原Fe2O3
+H2O,则E一定能还原Fe2O3
C.若D为CO,C能和E反应,则A一定为Na2O2
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某二元酸H2A在溶液中存在如下电离:H2A=H++HAˉ,HAˉ![]() H++A2ˉ,K=1.2×10-2。设NA为阿伏加德罗常数值。关于常温下0.01mol·L-1的H2A溶液,下列说法正确的是
H++A2ˉ,K=1.2×10-2。设NA为阿伏加德罗常数值。关于常温下0.01mol·L-1的H2A溶液,下列说法正确的是
A.![]()
B.pH<2
C.c(H+)=2c(H2A)+c(HAˉ)+c(OHˉ)
D.1L溶液中的H+数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题给要求填空
(1)某元素的基态原子最外层电子排布式为3s23p2,它的次外层上电子云形状有________种,原子中所有电子占有________个轨道,核外共有________种运动状态不同的电子。
(2)E原子核外占有9个轨道,且具有1个未成对电子,E离子结构示意图是_______。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是________,F2-的电子排布式是______。
(4)M能层上有________个能级,有________个轨道,作为内层最多可容纳________个电子,作为最外层时,最多可含有________个未成对电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用科学技术减少氮氧化物等物质的排放可促进社会主义生态文明建设。
(1)用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H=-662 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l) △H=-1248 kJ/mol
反应CH4(g)+2NO2(g)= N2(g) +CO2(g)+2H2O(l) △H=________kJ/mol
(2)氮氧化物可用碱溶液吸收。NO和NO2混合气体按一定比例被NaOH溶液完全吸收生成NaNO2和H2O,写出该反应的化学方程式________;若反应过程中消耗NaOH的物质的量为3 mol,则理论上被吸收的NO和NO2混合气体的总体积在标准状况下为________L。
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:
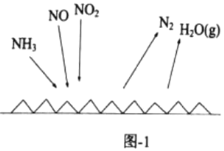
①由图1可知SCR技术中的还原剂为________。
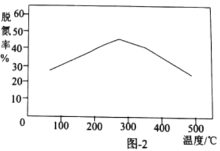
②一定时间内,用Fe作催化剂,氨气按一定的比例催化还原氮氧化物时,不同温度下的脱氮率如图2所示,温度高于300℃时,脱氮率随温度的升高而下降的原因可能是________。
(4)利用反应6NO2+8NH3=7N2+12H2O设计成原电池,既能减轻氮氧化物对环境的污染,又能充分利用化学能,装置如图3所示。
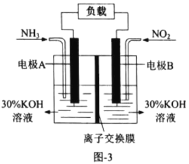
①电极B是________极(填“正”或者“负”)。
②A电极的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】格列本脲是一种降糖及利尿的药物,一种合成格列本脲的路线如图:
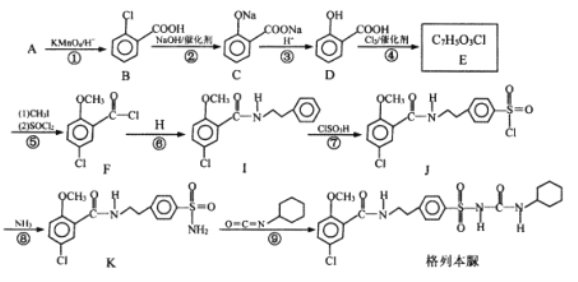
已知:(1)![]() (2)
(2)![]()
回答下列问题:
(1)B含有的官能团名称是_______,D的名称是__________。
(2)H的结构简式为__________。
(3)写出下列反应的反应类型:⑥__________,⑨__________。
(4)写出E与CH3I反应的化学反应方程式__________。
(5)符合下列要求的E的同分异构体有__________种。
①具有酯基、能发生银镜反应 ②遇FeCl3溶液显紫色
(6)以甲苯和![]() 为原料,其他无机试剂自选,参照上述格列本脲的合成路线,设计一条制备甲磺丁脲(
为原料,其他无机试剂自选,参照上述格列本脲的合成路线,设计一条制备甲磺丁脲(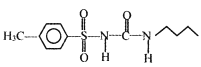 )的合成路线_____________.
)的合成路线_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,随着聚酯工业的快速发展,将氯化氢转化为氯气的技术成为科学研究的热点。传统的Deacon直接氧化法,按下列催化过程进行:4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g)
2Cl2(g)+2H2O(g)
(1)写出上述反应的平衡常数表达式K=___。
(2)生产过程中可使用CuCl2作催化剂,反应原理如下:
CuCl2(s)+![]() O2(g)=CuO(s)+Cl2(g) △H1=+63kJmol-1
O2(g)=CuO(s)+Cl2(g) △H1=+63kJmol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H2=-121kJmol-1
则4HCl(g)+O2(g)2Cl2(g)+2H2O(g)的△H=___kJmol-1。
(3)生产中反应温度通常控制在420℃左右,原因是___。在一定温度下,进一步提高HCl平衡转化率的方法是___(写出2种)。
(4)420℃时,将一定量的O2和HCl通入4L的恒容密闭容器中,反应过程中氧气的变化量如图所示,则0~20min平均反应速率v(HCl)为___molL-1·min-1。
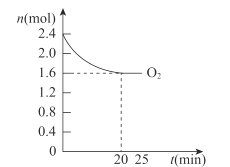
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价,如图所示为超氧化钾晶体的一个晶胞,则下列说法正确的是
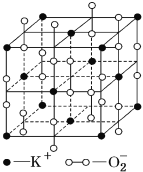
A. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个![]()
B. 晶体中每个K+周围有8个![]() ,每个
,每个![]() 周围有8个K+
周围有8个K+
C. 晶体中与每个K+距离最近的K+有8个,晶体中与每个![]() 距离最近的
距离最近的![]() 有6个
有6个
D. 晶体中其中0价氧和-2价氧的物质的量之比为1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com