
���� Fe��FeO��ϡ���ᷴӦ����FeSO4��n��H2SO4��=1L��1mol/L=1mol��������ȫ�ܽ⣬���Է�Ӧǰ����Һ����ı仯�������Һ��c��Fe2+��=0.3mol•L-1��n��Fe2+��=1L��0.3mol/L=0.3mol����������Ϊ������n��H2��=n��Fe�������n��Fe��+n��FeO��=n��Fe2+�����Դ˼��㣮
��� �⣺��1��FeO�����ᷴӦ��������������ˮ��ֻ��Fe�����ᷴӦ����H2���ʴ�Ϊ��H2��
��2����������Ӳ��μӷ�Ӧ����Ӧǰ����������ӵ�Ũ�Ȳ��䣬����1mol•L-1������Һ��֪����Ӧ����Һ��c��SO42-��=1mol/L���ʴ�Ϊ��1��
��3�������Һ��c��Fe2+��=0.3mol•L-1��n��Fe2+��=1L��0.3mol/L=0.3mol��n��H2��=n��Fe��=$\frac{4.48L}{22.4L/mol}$=0.2mol����Feԭ���غ��֪��n��Fe��+n��FeO��=n��Fe2+����n��FeO��=0.3mol-0.2mol=0.1mol����������FeΪ0.1mol��������Ϊ0.1mol��56g/mol=5.6g��
�𣺴˲����ѱ������������������5.6g��
���� ���⿼�黯ѧ��Ӧ����ʽ�ļ��㣬Ϊ��Ƶ���㣬���շ����ķ�Ӧ��ԭ���غ�Ϊ���Ĺؼ������ط�������������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ƿʵ��ǰ������ˮϴ�ɾ�����δ��� | |
| B�� | ���ݹ۲�Һ��ʱ���� | |
| C�� | ����Ͳ��ȡһ����Һ��ʱ������Һ����� | |
| D�� | ������ˮʱ���������˿̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
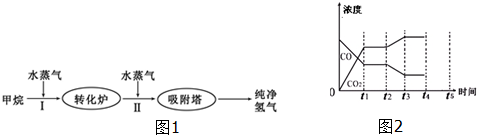
| �¶�/�� | 400 | 500 | 830 |
| ƽ�ⳣ��K | 10 | 9 | 1 |
| ʵ���� | ��Ӧ��Ͷ���� | ƽ��ʱH2Ũ�� | ���ջ�ų������� | ��Ӧ��ת���� |
| A | 1��1��0��0 | c1 | Q1 | ��1 |
| B | 0��0��2��2 | c2 | Q2 | ��2 |
| C | 2��2��0��0 | c3 | Q3 | ��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

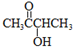 ��
�� CH3COO-+NH4++2Ag��+3NH3+H2O��
CH3COO-+NH4++2Ag��+3NH3+H2O�� ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������Zn���缫��Ӧ��Zn-2e-�TZn2+��
������Zn���缫��Ӧ��Zn-2e-�TZn2+���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

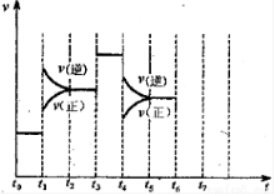
| ���� | ���� | ���� | �� |
| �۵㣨�棩 | -210 | -253 | -78 |
| �е㣨�棩 | -195 | -259 | -33 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ÿ����0.6mol H2������ԭ��ˮ������ĿΪ1.2NA | |
| B�� | ��2.7g Al�μӷ�Ӧʱ��ת�Ƶĵ�����ĿΪ0.3NA | |
| C�� | ��6.72L H2����ʱ����Ӧ��ת�Ƶĵ�����ĿΪ0.6NA | |
| D�� | ��Һ��ÿ����0.1mol AlO${\;}_{2}^{-}$��Na+����Ŀ������0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ù��˵ķ�������FeCl3��Һ��Fe��OH��3���� | |
| B�� | Fe��OH��3���徲�û�ֲ� | |
| C�� | HCl��SO2��Fe2+���������������л�ԭ�� | |
| D�� | CH3COONH4�ĵ��뷽��ʽΪ��CH3COONH4 CH3COO-+NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ڢ� | C�� | �٢ڢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com