
| N |
| NA |
| m |
| M |
| N |
| NA |
| 1 |
| 2 |
| n |
| V |
| 3.01×1023 |
| 6.02×1023mol-1 |
| 16g |
| 32g/mol |
| 9.03×1022 |
| 6.02×1023mol-1 |
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 0.075mol |
| 2L |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 丙烷进行氯代反应中,可分离出4种二氯代物A、B、C、D,分子式均为C3H6Cl2.当它们进一步氯代为三氯代物时,A只有一种三氯代物,B有2种三氯代物,C和D各有3种三氯代物,已知C具有不对称碳原子,试写出A、B、C、D的结构简式:A
丙烷进行氯代反应中,可分离出4种二氯代物A、B、C、D,分子式均为C3H6Cl2.当它们进一步氯代为三氯代物时,A只有一种三氯代物,B有2种三氯代物,C和D各有3种三氯代物,已知C具有不对称碳原子,试写出A、B、C、D的结构简式:A查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
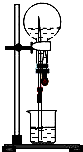 以下是针对喷泉实验所得溶液浓度问题的探讨,请根据题意回答问题.
以下是针对喷泉实验所得溶液浓度问题的探讨,请根据题意回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 一 | A | |||||||
| 二 | D | E | G | I | ||||
| 三 | B | C | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:
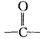 官能团.
官能团.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com