
���� ��1��Ca5F��PO4��3���Կ�������ơ������ƵĻ��������Ũ���ᷴӦ�������ᡢ�������HF��
����PԪ���غ�ɵù�ϵʽP4��2P2O5��4H3PO4�����ݴ˹�ϵʽ���㣻
��2���ȷ�����ָ�ù�����̿��������������ʯ�ڸ����»�õ����ף��������Ʊ����ᣬ��һ�������ɹ������SiF4��CO��β��Ӧ������Һ��������ͨ��NaClO��Һ�ɳ�ȥ���л�ԭ�Ե�PH3������Ӧ����P��NaCl��ˮ��
��� �⣺��1��Ca5F��PO4��3���Կ�������ơ������ƵĻ��������Ũ���ᷴӦ�������ᡢ�������HF����Ӧ����ʽΪ��Ca5F��PO4��3+5H2SO4=3H3PO4+5CaSO4+HF����
���Ƶõ�85%����Ʒ����xt����
P4��2P2O5��4H3PO4
124 392
1t��13% 85%x t
��124��392=1t��85%x t
���x=3.72t��
�ʴ�Ϊ��Ca5F��PO4��3+5H2SO4=3H3PO4+5CaSO4+HF����3.72��
��2������������������ᣬ�ȷ����Ṥ�ո��ӣ��ܺĸߣ��������ò�Ʒ���ȴ������٣�
�ʴ�Ϊ����Ʒ���ȸߣ�
���� �����ǶԻ�ѧ�뼼���Ŀ��飬�漰��ѧ���㡢��ѧ����ʽ��д������Ϣ����ȡӦ�ã��Ƕ�ѧ���ۺ������Ŀ��飬�ѶȽϴ�


 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д� Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ⷨ�������յķ���ʹ�������������е���Ѹ���ռ� | |
| B�� | �ϳɰ����յĿ���������������������Դ���Ӵ���ʳ�����ì�� | |
| C�� | �о�Ӱ�컯ѧ��Ӧ���ʵ����ض���߿��淴Ӧ���Ⱦ��о��������� | |
| D�� | ȼ�ϵ�ص�����ת��Ч�ʸ߾��й�����ǰ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��Ͳ | B�� |  �Թ� | C�� |  ������ | D�� |  ��Һ©�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڿ�����ȼ��ֻ���ɰ�ɫ�������ƹ��� | |
| B�� | ȼ�ŵ�þ������ʢ��������̼�ļ���ƿ�в��ܼ���ȼ�� | |
| C�� | ͭ�����Ȼ�����Һ��Ӧ���÷�Ӧ��������ӡˢ��·������� | |
| D�� | ���������ᷢ����Ӧ���ʲ�����������������Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
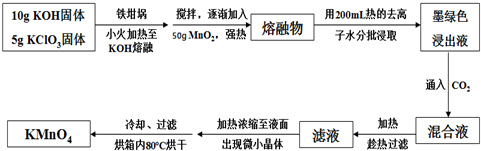
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
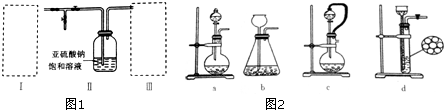
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܽ�ȣ�s�� | B�� | ���ʵ���Ũ�ȣ�c�� | C�� | ����������w�� | D�� | Ħ��������M�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com