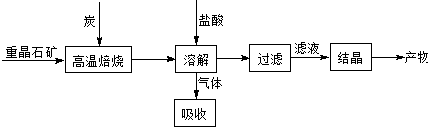
研究CO
2的利用对促进低碳社会的构建具有重要意义.
(1)将CO
2与焦炭作用生成CO,CO可用于炼铁等.
已知:Fe
2O
3(s)+3C(石墨)=2Fe(s)+3CO(g)△H
1=+489.0kJ?mol
-1 C(石墨)+CO
2(g)=2CO(g)△H
2=+172.5kJ?mol
-1则CO还原Fe
2O
3(s)的热化学方程式为
.
(2)二氧化碳合成甲醇是碳减排的新方向,将CO
2转化为甲醇的热化学方程式为:
CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g)△H
①该反应的平衡常数表达式为K=
.
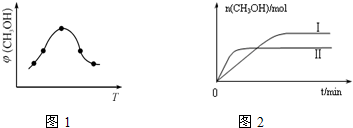
②取一定体积CO
2和H
2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应.反应过程中测得甲醇的体积分数φ(CH
3OH)与反应温度T的关系如图1所示,则该反应的△H
0(填“>”、“<”或“=”).
③在两种不同条件下发生反应,测得CH
3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为K
Ⅰ
K
Ⅱ(填“>”、“<”或“=”).
(3)以CO
2为原料还可以合成多种物质.
①工业上尿素[CO(NH
2)
2]由CO
2和NH
3在一定条件下合成,其反应方程式为
.当氨碳比
=3,达平衡时CO
2的转化率为60%,则NH
3的平衡转化率为
.
②用硫酸溶液作电解质进行电解,CO
2在电极上可转化为甲烷,该电极反应的方程式为
.


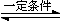 CO(NH2)2+H2O,
CO(NH2)2+H2O,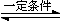 CO(NH2)2+H2O;
CO(NH2)2+H2O;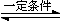 CO(NH2)2+H2O;40%;
CO(NH2)2+H2O;40%;