
ŗ¬11.2g KOHµÄĻ”ČÜŅŗÓė1L 0.1mol/LµÄH2SO4ČÜŅŗ·“Ó¦·Å³ö11.46kJµÄČČĮ棬ĻĀĮŠÄÜÕżČ·±ķŹ¾ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½ŹĒ£Ø£©
A£® KOH£Øaq£©+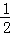 H2SO4£Øaq£©=1/2K2SO4£Øaq£©+H2O £Øl£©£»”÷H=﹣11.46kJ/mol
H2SO4£Øaq£©=1/2K2SO4£Øaq£©+H2O £Øl£©£»”÷H=﹣11.46kJ/mol
B£® 2KOH£Øs£©+H2SO4£Øaq£©=K2SO4£Øaq£©+2H2O £Øl£©£»”÷H=﹣114.6kJ/mol
C£® 2KOH£Øaq£©+H2SO4=K2SO4£Øaq£©+H2O £Øl£©£»”÷H=+114.6kJ/mol
D£® KOH £Øaq£©+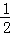 H2SO4£Øaq£©=
H2SO4£Øaq£©=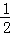 K2SO4£Øaq£©+H2O £Øl£©£»”÷H=﹣57.3kJ/mol
K2SO4£Øaq£©+H2O £Øl£©£»”÷H=﹣57.3kJ/mol
æ¼µć£ŗ ÖŠŗĶČČ£®
·ÖĪö£ŗ øł¾ŻĖį¼īµÄĪļÖŹµÄĮæÅŠ¶Ļ·“Ó¦µÄĒéæö£¬øł¾ŻÖŠŗĶČČŹĒÖøĻ”µÄĒæĖįŗĶĒæ¼ī·“Ӧɜ³É1molĖ®Ėł·Å³öµÄČČĮæĄ“ŹéŠ“ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½£®
½ā“š£ŗ ½ā£ŗ11.2g¼“0.2molKOHµÄĻ”ČÜŅŗÓė1L”¢0.1mol/LµÄH2SO4ČÜŅŗ·“Ó¦·Å³ö11.46kJµÄČČĮ棬ŹµÖŹŹĒÉś³É0.2molĖ®·Å³ö11.46kJµÄČČĮ棬¶ųÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½±ŲŠė±£³ÖÉś³ÉĖ®µÄĪļÖŹµÄĮæĪŖ1mol£®
A”¢Éś³É1molĖ®·Å³öµÄČČĮæ»įøßÓŚ11.46kJ£¬¹ŹA“ķĪó£»
B”¢ĒāŃõ»Æ¼ŲÓ¦ŹĒČÜŅŗ£¬²»ŹĒ¹ĢĢ壬¹ŹB“ķĪó£»
C”¢ÖŠŗĶ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬²»ŹĒĪüČČ·“Ó¦£¬¹ŹC“ķĪó£»
D”¢KOHµÄĻ”ČÜŅŗÓėH2SO4ČÜŅŗ·“Ӧɜ³É0.2molĖ®·Å³ö11.46kJµÄČČĮæ£¬Éś³É1molĖ®»į·Å³ö57.3KJµÄÄÜĮ棬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ£ŗ ±¾Ģāæ¼²éÖŠŗĶČȵÄøÅÄīŅŌ¼°ČČ»Æѧ·½³ĢŹ½µÄŗ¬Ņ壬æÉŅŌøł¾ŻĖłŃ§ÖŖŹ¶Ą“»Ų“š£¬ÄŃ¶Č²»“ó£®


 ÓŵČÉśĢāæāĻµĮŠ“š°ø
ÓŵČÉśĢāæāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČĻÕę¹Ū²ģĻĀĮŠ×°ÖĆ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
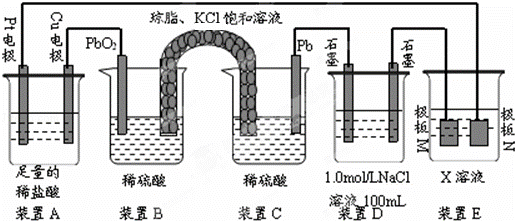
£Ø1£©×°ÖĆBÖŠPbO2ÉĻ·¢ÉśµÄµē¼«·“Ó¦·½³ĢŹ½ĪŖ £®
£Ø2£©×°ÖĆAÖŠ×Ü·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £®
£Ø3£©Čō×°ÖĆEÖŠµÄÄæµÄŹĒŌŚCu²ÄĮĻÉĻ¶ĘŅų£¬ŌņXĪŖ £¬¼«°åNµÄ²ÄĮĻĪŖAg£®Čō×°ÖĆEµÄÄæµÄŹĒŃéÖ¤½šŹōµÄµē»Æѧ·ĄøÆ£¬Ōņ¼«°åNµÄ²ÄĮĻĪŖ £®
£Ø4£©µ±×°ÖĆAÖŠCuµē¼«ÖŹĮæøıä6.4gŹ±£¬×°ÖĆDÖŠ²śÉśµÄĘųĢåĢå»żĪŖ L£Ø±ź×¼×“æöĻĀ£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĮ½øöĆܱÕČŻĘ÷ÖŠ£¬·Ö±š³äÓŠÖŹĮæĻąĶ¬µÄ¼×”¢ŅŅĮ½ÖÖĘųĢ壬ČōĮ½ČŻĘ÷µÄĪĀ¶ČŗĶŃ¹Ēæ¾łĻąĶ¬£¬ĒŅ¼×µÄĆܶȓóÓŚŅŅµÄĆÜ¶Č£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | ¼×µÄ·Ö×ÓŹż±ČŅŅµÄ·Ö×ÓŹż¶ą |
| ”” | B£® | ¼×µÄĪļÖŹµÄĮæ±ČŅŅµÄĪļÖŹµÄĮæÉŁ |
| ”” | C£® | ¼×µÄĦ¶ūĢå»ż±ČŅŅµÄĦ¶ūĢå»żŠ” |
| ”” | D£® | ¼×µÄĻą¶Ō·Ö×ÓÖŹĮæ±ČŅŅµÄĻą¶Ō·Ö×ÓÖŹĮ抔 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻąĶ¬ÖŹĮæµÄĖÄ·ŻĶʬ£¬·Ö±šÖĆÓŚ×ćĮæµÄĻĀĮŠĖįÖŠ£¬ĖłµĆµ½µÄĘųĢåµÄĪļÖŹµÄĮæ×ī¶ąµÄŹĒ£Ø£©
A£® Ļ”ĮņĖį B£® ÅØĮņĖį C£® Ļ”ĻõĖį D£® ÅØĻõĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
°ŃSO2ĶØČėFe£ØNO3£©3ČÜŅŗÖŠ£¬ČÜŅŗÓÉ»ĘÉ«±äĪŖĒ³ĀĢÉ«£¬µ«Į¢¼“ÓÖ±äĪŖ»ĘÉ«£¬“ĖŹ±ČōµĪČėBaCl2ČÜŅŗ£¬Ōņ»į²śÉś°×É«³Įµķ£®ŌŚÉĻŹöŅ»ĻµĮŠ±ä»Æ¹ż³ĢÖŠ£¬×īÖÕ±»»¹ŌµÄŹĒ£Ø£©
A£® SO2 B£® NO3﹣ C£® Fe3+ D£® Fe2+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øßĢśµē³ŲŹĒŅ»ÖÖŠĀŠĶæɳäµēµē³Ų£¬øƵē³Ų³¤Ź±¼ä±£³ÖĪČ¶ØµÄ·ÅµēµēŃ¹£®øßĢśµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ3Zn+2K2FeO4+8H2O 3Zn£ØOH£©2+2Fe£ØOH£©3+4KOH£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø£©
3Zn£ØOH£©2+2Fe£ØOH£©3+4KOH£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø£©
A£® ·ÅµēŹ±øŗ¼«·“Ó¦ĪŖ£ŗZn﹣2e﹣+2OH﹣=Zn£ØOH£©2
B£® ³äµēŹ±Ńō¼«·“Ó¦ĪŖ£ŗFe£ØOH£©3﹣3e﹣+5OH﹣=FeO42﹣+4H2O
C£® ·ÅµēŹ±Ćæ×ŖŅĘ1 molµē×Ó£¬Õż¼«ÓŠ1mol K2FeO4±»»¹Ō
D£® ·ÅµēŹ±Õż¼«ø½½üČÜŅŗµÄpHֵɿøß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼£ŗa”¢b”¢c”¢d¾łĪŖ²¬µē¼«£¬¹©Ń”ŌńµÄĖÄ×éµē½āŅŗČēĻĀ£ŗ
×é A B C D
¼×²Ū NaOH AgNO3 H2SO4 NaCl
ŅŅ²Ū CuSO4 CuCl2 AgNO3 AgNO3
ŅŖĒóĀś×ćµÄĢõ¼žŹĒ£ŗ
£Øa£©¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬼ײŪµē½āŅŗpHÖµÉĻÉż£¬ŅŅ²Ūµē½āŅŗµÄpHÖµĻĀ½µ
£Øb£©a”¢dĮ½¼«·ÅµēĄė×ÓµÄĪļÖŹµÄĮæĻąµČ
ĒėĢīŠ“ĻĀĮŠæÕøń£ŗ
£Ø1£©Ó¦Ń”ÓƵĵē½āŅŗŹĒÄÄŅ»×éD£»£ØĢī×ÖÄø£©
£Ø2£©¼×²ŪµÄµē½ā·½³ĢŹ½ £®
£Ø3£©µ±a¼«Īö³ö3.55gµē½ā²śĪļŹ±£¬d¼«ÉĻ½«Īö³ö gĪļÖŹ£®

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻąĶ¬Ģå»żµÄKI”¢Na2S”¢FeBr2ČÜŅŗ£¬·Ö±šĶØČė×ćĮæµÄCl2£¬µ±·“Ó¦Ē”ŗĆĶź³ÉŹ±£¬ĻūŗÄCl2µÄĢå»żĻąĶ¬£ØĶ¬ĪĀ”¢Ķ¬Ń¹Ģõ¼žĻĀ£©£¬ŌņKI”¢Na2S”¢FeBr2ČÜŅŗµÄĪļÖŹµÄĮæÅضČÖ®±ČŹĒ£Ø””””£©
| ”” | A£® | 1£ŗ1£ŗ2 | B£® | 2£ŗ1£ŗ3 | C£® | 6£ŗ3£ŗ2 | D£® | 3£ŗ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹Ų»ÆѧÓĆÓļ±ķŹ¾ÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | ŅŅČ²µÄµē×ÓŹ½H£ŗC£ŗ£ŗ£ŗC£ŗH | B£® |
|
| ”” | C£® | ¶Ō¼×»ł±½¼×“¼µÄ½į¹¹¼ņŹ½£ŗ | D£® | ŅŅ“¼·Ö×ӵıȥżÄ£ŠĶ£ŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com