
苯螨特(Benzomate)是一种用于防治红蜘蛛的新型农药,一种合成苯螨特的合成路线流程图如下:
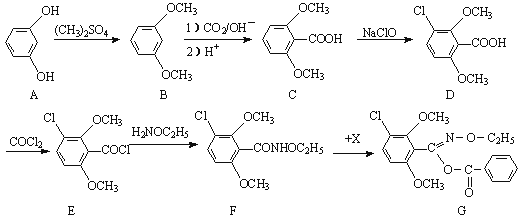
请回答下列问题:
(1)A→B反应类型是 。
(2)化合物C中含氧官能团名称是 和 。
(3)化合物X的分子式为:C7H5OCl,,则X的结构简式为 。
(4)C的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应也能与FeCl3溶液发生显色反应。
Ⅱ.分子中有4种不同化学环境的氢。
写出一种符合条件的同分异构体的结构简式: 。

(5)根据已有知识并结合相关信息,写出以 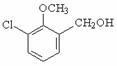 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备
的合成路线流程图(无机试剂任用)。
已知:CH2=CHCOOH 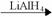 CH2=CHCH2OH。
CH2=CHCH2OH。
合成路线流程图示例如下:
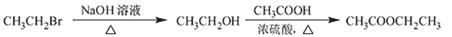
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
脱水偶联反应是一种新型的直接烷基化反应,例如:

Ⅲ
(1)化合物Ⅰ的分子式为________,1 mol该物质完全燃烧最少需要消耗________mol O2。
(2)化合物Ⅱ可使________溶液(限写一种)褪色;化合物Ⅲ(分子式为C10H11Cl)可与NaOH水溶液共热生成化合物Ⅱ,相应的化学方程式为__________________________________________________。
(3)化合物Ⅲ与NaOH乙醇溶液共热生成化合物Ⅳ,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为1:1:1:2,Ⅳ的结构简式为____________________________________________________。
(4)由CH3COOCH2CH3可合成化合物Ⅰ。化合物Ⅴ是CH3COOCH2CH3是一种无支链同分异构体,碳链两端呈对称结构,且在Cu催化下与过量O2反应生成能发生银镜反应的化合物Ⅵ。Ⅴ的结构简式为________________,Ⅵ的结构简式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的检验,其结论一定正确的是( )
A.某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他
现象,说明该溶液中一定含有SO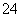
B.某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一
定含有 CO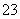 或 HCO
或 HCO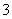
C.某溶液中加盐酸产生刺激性气味的无色气体,该气体能使品红溶液褪色,说明该溶
液中一定含有SO
D.取少量久置的Na2SO3样品于试管中加水溶解,再加入足量盐酸有气体产生,然后加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是
A.FeCl3溶液中加入过量的锌粉:Zn +2Fe3+=Zn2++2Fe2+
B.NH4Al(SO4)2中加入过量的NaOH溶液:Al3++4OH-=AlO2-+2H2O
C.(CH3COO)2Ba中加入稀硫酸:Ba2+ + SO42- = BaSO4↓
D.用惰性电极电解Cu(NO3)2溶液:2Cu2+ +2H2O  2Cu+ O2↑+ 4H+
2Cu+ O2↑+ 4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
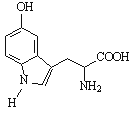
5—羟色胺对人体睡眠具有调节作用,其结构简式如右图所示。下列有关5—羟色胺说法错误的是
A.该有机物分子式为C11H12N2O3
B.该有机物分子中所有原子不可能共平面
C.分子中含有1个手性碳原子
D.1mol该物质最多可与4molH2或1molBr2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
(一)乙酸正丁酯的制备
①在干燥的50mL圆底烧瓶中,加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应
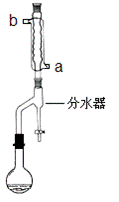
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用10 mL的水洗涤。有机层继续用10 mL10%Na2CO3洗涤至中性,再用10 mL 的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥。
③将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集125~127 ℃的馏分,得11.6 g乙酸正丁酯
请回答有关问题。
(1)冷水应该从冷凝管 ___________(填a或b)管口通入。
(2)步骤①中不断从分水器下部分出生成的水的目的是_________________________
步骤①中判断反应终点的依据是_____________________________________。
(3)产品的精制过程步骤②中,第一次水洗的目的是_____________________________,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是_________________________________。
(4)下列关于分液漏斗的使用叙述正确的是____
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.装液时,分液漏斗中液体的总体积不得超过其容积的2/3
C.萃取振荡操作应如右图所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
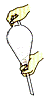
(5)步骤③的常压蒸馏,需收集126℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是_________________________
(6)该实验过程中,生成乙酸正丁酯(式量116)的产率是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理知识回答下列有关碳和碳的化合物的问题:
(1)汽车尾气的主要污染物是NO以及燃料燃烧不完全所产生的CO,它们是现代化城市的重要大气污染物,为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应△H<0). 在2 L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
|
T/℃ n/mol | NO | CO | E | F |
| 初始 | 0.100 | 0.100 | 0 | 0 |
| T1 | 0.020 | 0.020 | 0.080 | 0.040 |
| T2 | 0.010 | 0.010 | 0.090 | 0.045 |
①请结合上表数据,写出NO与CO反应的化学方程式 .
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2,根据表中数据计算K1= 。根据表中数据判断,温度T1和T2的关系是(填序号)__________。
A.T1>T2B.T1<T2 C.T1=T2 D.无法比较
(2)反应生成的气体E经常用氢氧化钠来吸收,现有0.4molE,若用200mL 3mol/L NaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为: .
(3)已知CH4、H2和CO的燃烧热分别为890.3kJ/mol,285.8 kJ/mol和283.0 kJ/mol,工业上利用天然气(主要成分是CH4)与CO2进行高温重整制备CO和H2,写出该反应的热化学方程式: .
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用 Li2CO3 和 Na2CO3 的熔融盐混合物作电解质,CO为负极燃气,空气与CO2 的混合气为正极助燃气,制得在 650 ℃下工作的燃料电池,写出其负极和正极电极反应方程式:负极: ;正极: .
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组为探究铜与浓硫酸的反应,用如图所示装置进行有关实验。实验中甲同学将a g铜片和12 mL 8 mol·L-1浓H2SO4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。

请回答下列问题:
(1)请写出Cu与浓H2SO4反应的化学方程式:____________。
(2)装置D内盛品红溶液,当C中气体集满后,D中有可能观察到的现象是______________________________________________。
实验装置D有可能造成环境污染,试用最简单的方法加以解决(实验用品自选)__________________________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B装置中的现象是____________________________________。
(4)F中应放置的液体是________(填序号)。
A.饱和Na2SO3溶液
B.酸性KMnO4溶液
C.浓溴水
D.饱和NaHSO3溶液
(5)为什么有一定量的余酸,但未能使Cu完全溶解,你认为原因是_____________________________________________________。
(6)下列足量药品能够用来证明反应结束后的烧瓶中确有余酸的是________(填序号)。
A.铁粉 B.BaCl2溶液
C.Ag D.Na2CO3溶液
(7)甲同学向A中反应后的溶液中通入一种气 体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是________(填名称),反应方程式是_____________________________________________。
体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是________(填名称),反应方程式是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学实验事实及其结论都正确的是( )。
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以与NaOH溶液及HF溶液反应 | SiO2属于两性氧化物 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com