
| A、金属铝有好的导热性,常用铝箔做包装材料 |
| B、Al2O3是两性氧化物,常用其作耐火材料 |
| C、Al(OH)3能与胃液中的盐酸反应,可用其制作中和胃酸的药物 |
| D、明矾能吸附水中的悬浮物,可用其作净水剂 |


科目:高中化学 来源: 题型:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| 5n(NO)(mol) | 0.020 | 0.010 | 0.006 | 0.004 | 0.004 | 0.004 |
查看答案和解析>>
科目:高中化学 来源: 题型:
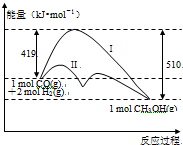 反应CO(g)+2H2(g)?CH3OH(g)过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
反应CO(g)+2H2(g)?CH3OH(g)过程中的能量变化情况如图所示,曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )| A、该反应的△H=+91 kJ/mol |
| B、加入催化剂,该反应的△H变小 |
| C、如果该反应生成液态CH3OH,则△H变大 |
| D、反应物的总能量大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性氧化物 过氧化钠 Na2O2 |
| B、碱 纯碱 Na2CO3 |
| C、金属氧化物 氧化铁 FeO |
| D、非金属氧化物 三氧化硫 SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| V2O5 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
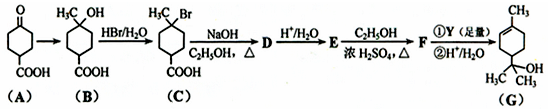
| ①R′MgBr(足量) |
| ②H+/H2O |
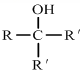
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=2的可乐中c(H+)是pH=3的柠檬水中c(H+)的10倍 |
| B、体积相同、pH相同的醋酸和盐酸完全溶解等量的镁粉,后者用时少 |
| C、pH=10的NaOH溶液与pH=12的NaOH的溶液等体积混合后,溶液的pH=11 |
| D、若V1LpH=11的NaOH溶液与V2LpH=3的HA溶液混合后显中性,则V1≤V2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com