
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA
B.l mol Fe(NO3)3与足量HI溶液反应时转移的电子数为3NA
C.1 mol Na2O2固体中含离子总数为4NA
D.常温下,1 mol Fe与过量浓HNO3反应,转移电子的数目为3 NA
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 需要加热方能发生的反应一定是吸热反应 B.放热反应在常温下一定很容易发生
C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小
D.化学反应只生成新物质,没有能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法错误的是
| X | Y | ||
| W | Z | ||
| T |
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.物质W3X4中,每个原子最外层均达到8电子稳定结构
C.X、Y和氢形成的化合物中可能既有离子键、又有共价键
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学用语的表示正确的是
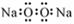
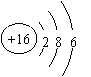 A.过氧化钠电子式: B.质子数35、中子数45的溴原子:
A.过氧化钠电子式: B.质子数35、中子数45的溴原子: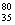 Br
Br
C.硫离子结构示意图: D.HCN的结构式:H—N=C
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解,不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6[来源:学科网ZXXK] | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6 min的平衡反应速率:v(H2O2)≈3.3×10-2 mol/(L·min)
B.6~10 min的平衡反应速率:v(H2O2)<3.3×10-2 mol/(L·min)
C.反应到6 min时,c(H2O2)=0.30 mol/L
D.反应到6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
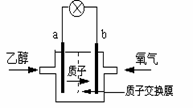
圣路易斯大学研制的新型乙醇燃料电池, 用能传递质子(H+)的介质作溶剂, 反应为C2H5OH+3O2→2CO2+3H2O,下图是该电池的示意图,下列说法正确的是
A.a极为电池的正极
B.电池正极的电极反应为:4H+ + O2 + 4e-=== 2H2O
C.电池工作时电流由a极沿导线经灯泡再到b极
D.电池工作时,1mol乙醇被氧化时就有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨是人类科学技术上的一项重大突破,其反应原理为:N 2(g)+3H2(g)
2(g)+3H2(g)
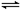 2NH3(g),一种工业合成氨,进而合成尿素的的简易流程图如下:
2NH3(g),一种工业合成氨,进而合成尿素的的简易流程图如下:
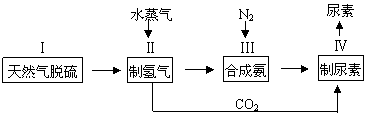 |
(1)步骤II中制氢气原理如下:
CH4(g)+H2O(g)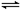 CO(g)+3H2(g) CO(g)+H2O(g)
CO(g)+3H2(g) CO(g)+H2O(g)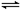 CO2(g)+H2(g)
CO2(g)+H2(g)
恒容容器中,对于以上反应,能加快反应速率的是 。
a. 升高温度 b. 充入He c. 加入催化剂 d. 降低压强
(2)天然气中的H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为
。
(3)CO2和H2在高温、高压、催化剂条件下可合成CH3CH2OH,反应的化学方程式
_________________________________。以CH3CH2OH 、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池,该电池中负极上的电极反应
、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池,该电池中负极上的电极反应 式是:_________________________。
式是:_________________________。
 (4)已知尿素的结构简式为H2N-
(4)已知尿素的结构简式为H2N-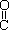 -NH2,请写出尿素的同分异构体中含有离子键的化学式 。
-NH2,请写出尿素的同分异构体中含有离子键的化学式 。
(5)已知CO2+ 2NH3 CO(NH2)2 + H2O,若合成尿素的流程中转化率为80%时,100吨甲烷为原料能够合成 吨尿素。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为六种短周期元素的部分性质:
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.74 | 0.75 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
下列有关说法错误的是( )
A.X与Y可以形成阴离子XY32-
B.元素R的氧化物对应水化物一定为强酸
C.Z的氢化物的沸点比T的氢化物的沸点高
D.由X形成的化合物QX和XR4,其晶体类型不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
A.①③⑤ B.②④⑥ C.②③④ D.①③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com