

| A. | 用水润湿的 pH 试纸测量某溶液的 pH | |
| B. | 用量筒量取 20 mL 0.5000 mol/LH2SO4溶液于烧杯中,加水 80 mL,配制成 0.1000 mol/LH2SO4溶液 | |
| C. | 实验室用图Ⅰ所示装置制取并收集少量氨气 | |
| D. | 实验室用图Ⅱ所示装置除去Cl2中的少量HCl |
分析 A.用水润湿pH试纸会导致溶液浓度偏低;
B.配制一定物质的量浓度溶液用容量瓶;
C.浓氨水和CaO混合得到氨气,氨气密度小于空气且常温下和空气不反应;
D.饱和食盐水抑制氯气溶解,HCl易溶于水.
解答 解:A.用水润湿pH试纸会导致溶液浓度偏低,可能会导致某些溶液pH变化,如用湿润的试纸测定稀盐酸溶液,溶液浓度变小,则测定pH值偏大,故A错误;
B.配制一定物质的量浓度溶液用容量瓶,需要将浓硫酸在烧杯中稀释,然后冷却至室温后再转移到容量瓶中,故B错误;
C.浓氨水和CaO混合得到氨气,氨气密度小于空气且常温下和空气不反应,但收集氨气时不能用橡皮塞塞住试管,否则压强过大会导致安全事故,故C错误;
D.饱和食盐水抑制氯气溶解,HCl易溶于水,所以实验室用图Ⅱ所示装置除去Cl2中的少量HCl,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及pH试纸的使用、溶液配制、气体制备和收集、除杂等知识点,明确实验原理及物质性质是解本题关键,注意从实验操作、物质性质、实验原理方面分析判断,易错选项是C.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
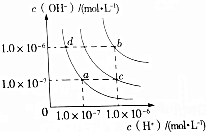
| A. | a点对应温度条件下,将pH=x的氨水稀释10倍后,其pH=y,则x=y+1 | |
| B. | 纯水仅升高温度,可从d点变到b点 | |
| C. | c点对应温度条件下醋酸的电离常数比a点对应温度条件下醋酸的电离常数大 | |
| D. | b点对应温度条件下,0.5mol•L-1的H2SO4溶液与1mol•L-1的KOH溶液等体积混合,充分反应后,所得溶液的c(H+)=10-7mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食用白糖的主要成分是葡萄糖 | |
| B. | 对“地沟油”进行分馏可得到汽油 | |
| C. | NH3易液化,可作制冷剂 | |
| D. | 地质灾害发生后,防疫人员常用明矾对饮用水进行消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
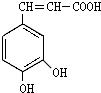 咖啡酸(结构如图)存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
咖啡酸(结构如图)存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
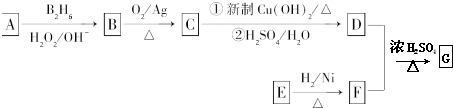
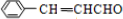 .
.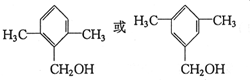 .
.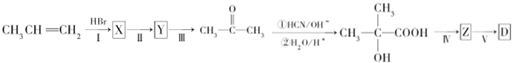
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | 氢氧化铁溶胶、水玻璃、淀粉溶液均具有丁达尔效应 | |
| C. | 12月2日我国发射的“嫦娥三号”卫星中使用的碳纤维,是一种新型无机非金属材料 | |
| D. | 只要符合限量,“食用色素”、“碘元素”、“亚硝酸盐”可以作为某些食品的添加剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
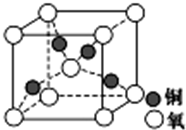 目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破.用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破.用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于10.0mL | B. | 小于10.0mL | C. | 等于10.0mL | D. | 等于11.0mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,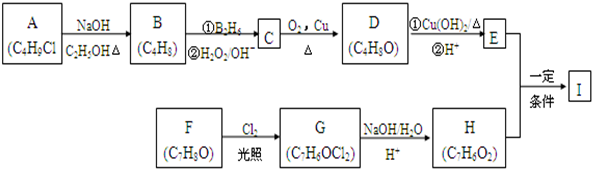
 ,该反应类型为取代反应.
,该反应类型为取代反应. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com