
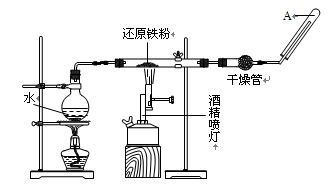
科目:高中化学 来源:不详 题型:实验题
 5.00mL加入过量的c1mol·L-lV1mL碘溶液,充分反应后再用c2mol·L-1Na2S2O3溶液滴定过量的碘,终点时消耗V2mLNa2S2O3溶液。
5.00mL加入过量的c1mol·L-lV1mL碘溶液,充分反应后再用c2mol·L-1Na2S2O3溶液滴定过量的碘,终点时消耗V2mLNa2S2O3溶液。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用食盐水除水垢 |
| B.用加热的方法给聚乙烯塑料袋封口 |
| C.用铅笔芯代替石墨试验导电性 |
| D.用灼烧的方法区别羊毛线和棉线 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某固体加入稀盐酸,产生无色且使澄清石灰水变浑浊的气体,证明该固体一定含CO32- |
| B.检验烧碱溶液中是否含Cl-,先加稀盐酸,再加AgNO3溶液,产生白色沉淀 |
C.某溶液中滴加BaCl2溶液,再加稀HNO3,产生白色沉淀,原溶液中一定含SO |
| D.某溶液中滴入KSCN溶液无明显变化,再加入氯水呈红色,原溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用加入适量铜粉的方法除去Cu(NO3)2溶液中混有的AgNO3 |
B.向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液的SO - - |
| C.用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 |
| D.先后添加酚酞试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
查看答案和解析>>
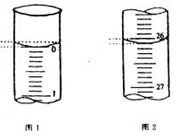
科目:高中化学 来源:不详 题型:实验题
| A.称量KOH固体时,直接用纸称量; |
| B.KOH固体溶解后,未完全冷却就转移至容量瓶中; |
| C.定容时,俯视容量瓶标线; |
| D.配制溶液前,容量瓶未完全干燥; |
查看答案和解析>>
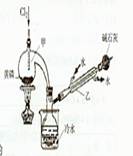
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
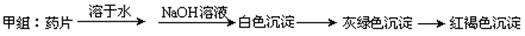 甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果,
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果, 
 进行实验验证:________________________________
进行实验验证:________________________________| 序号 | V(KMnO4)初 | V(KMnO4)终 | V(KMnO4) |
| 1 | 2.24mL | 14.25mL | 12.01mL |
| 2 | 0.30mL | 12.72mL | 12.42mL |
| 3 | 0.50mL | 12.53 | 12.03mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
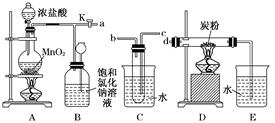
 斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,等分层后取上层液
斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,等分层后取上层液 和下层液,呈黄绿色的是________(填“上层液”或“下层液”),能使有色布条褪色的是________(填“上层液”或“下层液”).
和下层液,呈黄绿色的是________(填“上层液”或“下层液”),能使有色布条褪色的是________(填“上层液”或“下层液”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com