
【题目】在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是

A. a点对应的无色溶液中能大量存在:Fe3+、Na+、Cl-、SO42-
B. b点对应的溶液中能大量存在:NH4+、Ca2+、AlO2-、I-
C. c点对应的溶液中能大量存在:Na+、Ba2+、Cl-、CO32-
D. d点对应的溶液中能大量存在:Na+、K+、SO32-、Cl-
科目:高中化学 来源: 题型:
【题目】如图是某种有机物分子的球棍模型图。图中的“棍”代表单键或双键,不同大小的“球”代表三种不同的短周期元素的原子。对该有机物的叙述不正确的是( )
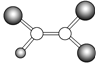
A.该有机物可能的分子式为C2HCl3
B.该有机物分子中一定有![]()
C.该有机物分子中的所有原子在同一平面上
D.该有机物可以由乙炔和氯化氢加成反应得到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
选项 | 微粒组 | 所加试剂 | 离子方程式 |
A | NH | 少量Ba(OH)2溶液 | 2NH |
B | Mg2+、Cl-、HCO | 过量NaOH溶液 | Mg2++2HCO |
C | Fe2+、NO | NaHSO4溶液 | HSO |
D | K+、CO | 通入少量CO2 | CO |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的可再生能源。
(1)已知2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH =a KJ/mol
CO(g)+2H2(g)=CH3OH(g) ΔH =b KJ/mol
试写出由CH4和O2制取甲醇的热化学方程式: 。
(2)还可以通过下列反应制备甲醇:CO(g)+2H2(g) ![]() CH3OH(g)。
CH3OH(g)。
甲图是反应时CO和CH3OH(g)的浓度随时间的变化情况。从反应开始到达平衡,用H2表示平均反应速率v(H2)= 。
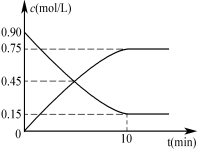
甲图
(3)在一容积可变的密闭容器中充入10 mol CO和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如乙图所示。

乙图
①下列说法能判断该反应达到化学平衡状态的是_______。(填字母)
A.H2的消耗速率等于CH3OH的生成速率的2倍 B.H2的体积分数不再改变
C.体系中H2的转化率和CO的转化率相等
D.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA________PB(填“>、<、=”)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10molCO和20 molH2,则在平衡状态B时容器的体积V(B)= L。
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)。若KOH溶液足量,则写出电池总反应的离子方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难溶电解质的溶解平衡属于化学平衡的一种。
(1)已知H2A在水中存在以下平衡:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。常温下CaA的饱和溶液中存在以下平衡:CaA(s)
H++A2-。常温下CaA的饱和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq) ΔH>0,则该饱和溶液呈________性(填“酸”、“碱”或“中”),将溶液放入冰水浴中,则CaA的Ksp将_____(填“增大”、“减小”或“不变”,下同);滴加少量浓盐酸,c(Ca2+)________。
Ca2+(aq)+A2-(aq) ΔH>0,则该饱和溶液呈________性(填“酸”、“碱”或“中”),将溶液放入冰水浴中,则CaA的Ksp将_____(填“增大”、“减小”或“不变”,下同);滴加少量浓盐酸,c(Ca2+)________。
(2)含有Cr2O72-的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O72-。为使废水能达标排放,做如下处理:Cr2O72-Cr3+、Fe3+Cr(OH)3、Fe(OH)3。欲使10 L该废水中的Cr2O72-完全转化为Cr3+,则理论上需要加入________g FeSO4·7H2O。若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为________mol·L-1(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向5 mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴加一滴Na2S溶液并振荡,沉淀又变成黑色。根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A. AgCl=AgI=Ag2S B. AgCl<AgI<Ag2S
C. AgCl>AgI>Ag2S D. AgI>AgCl>Ag2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色的强碱性溶液中,能大量共存的是( )
A.Na+、Al3+、NO3-、Cl- B.K+、Na+、Cl-、AlO2-
C.Fe2+、K+、SO42-、Cl- D.Na+、HCO3-、K+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015安徽理综化学】下列有关说法正确的是 ( )
A.在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解
B.Fe(OH)3胶体无色、透明,能发生丁达尔现象
C.H2、SO2、CO2三种气体都可用浓硫酸干燥
D.SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期A、B、C、D、E5种主族元素,-子序数依次增大,A是元素周期表中原子半径最小元素,B元素最高价氧化物分子式为B2O5;C的阴离子和D的阳离子具有相同的电子层结构,E的L层电子数等于K、M两个电子层上电子数之和。
(1)元素:A为 ,B为
(2)E在周期表中的位置为
(3)C、D两元素的单质反应,生成一种淡黄色的固体F,则F的化学式为是 ,属于 化合物(填“离子”或“共价”),该化合物中阴阳离子数比为
(4)单质C怎能溶于元素B最高价氧化物对应水化物的稀溶液,请写出该反应离子方程式
(5)E 的一种氧化物为酸雨的“罪魁祸首”。设计一实验证明某气体为E 的该氧化物,并写出该氧化物与足量NaOH的反应离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com