
下列反应的离子方程式正确的是( )
A.NaHCO3溶液中加入盐酸:CO32-+ 2H+ = CO2↑+ H2O
B.紫色石蕊试液中滴入氢硫酸变红的原因是:H2S 2H+ + S2-
2H+ + S2-
C.将NaHSO4溶液滴入Ba(OH)2溶液中至pH=7:2H+ + SO42-+ 2OH-+ Ba2+ = BaSO4↓+ 2H2O
D.电解CuSO4溶液:Cu2+ + 2H2O Cu + O2↑+ 4H+
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列化学工业原理对应不正确的是
|
|
|
|
| |
| 化工 | 氯碱工业 | 高炉炼铁 | 铜的精炼 | 生产漂白粉 |
| 原理 | 2H2O+2NaCl | 3CO+Fe2O3 | 阴极: Cu-2e-=Cu2+ | 2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O |
| A | B | C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NH3和HCl都能用来作喷泉实验.若在同温同压下用等体积烧瓶,一个收集满NH3,另一个收集HCl气体未满,做喷泉实验,如图所示,喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑溶质的扩散及静止时液面高度的影响)( )

A、溶质的物质的量浓度相同、溶质的质量分数不同
B、溶质的质量分数相同,溶质的物质的量浓度不同
C、溶质的物质的量浓度和溶质的质量分数都不同
D、溶质的物质的量浓度和溶质的质量分数都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
用稀H2SO4、NaOH溶液和金属铝为原料制取Al(OH)3。甲、乙、丙三个学生的制备途径分别是
甲:Al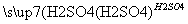 Al2(SO4)3
Al2(SO4)3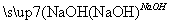 Al(OH)3
Al(OH)3
乙:Al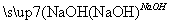 NaAlO2
NaAlO2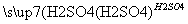 Al(OH)3
Al(OH)3
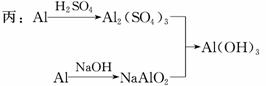
若要得到等量的Al(OH)3,则( )
A.三者消耗的原料相同
B.甲消耗的原料的总物质的量最多
C.乙消耗的原料的总物质的量最少
D.丙消耗的原料的总物质的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

回答下列问题:
(1)写出反应④的离子方程式______________________________________________。
(2)填写下表中的空白。(注:若混合物中不存在该成分,则“质量”栏中填“0”;画斜线的表格不需填写)
| 成分 | 质量 | 判断依据或计算推理过程 |
|
| ||
| (NH4)2SO4 | ||
| MgCl2 | ||
| FeCl2 | ||
| AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
体积恒定的密闭容器中,反应2SO2(g)+O2(g) 2SO3(g) △H <0达平衡后,采用下列措施一段时间后,既能增大逆反应速率又能使平衡向正方向移动的是
2SO3(g) △H <0达平衡后,采用下列措施一段时间后,既能增大逆反应速率又能使平衡向正方向移动的是
A.通入大量O2 B.增大容器容积 C.移去部分SO3 D.降低体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,将纯Fe棒和石墨棒插入1 L饱和NaCl溶液中。下列说法正确的是( )
A.M接负极,N接正极,当两极产生气体总量为22.4 L(标准状况)时,生成
1 mol NaOH
B.M接负极,N接正极,在溶液中滴人酚酞试液,C电极周围溶液变红
C.M接负极,N接正极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段
时间后,烧杯中产生蓝色沉淀
D.M接电源正极,N接电源负极,将C电极换成Cu电极,电解质溶液换成CuSO4 溶液,则可实现在铁上镀铜
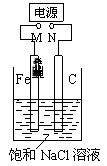
查看答案和解析>>
科目:高中化学 来源: 题型:
同素异形体相互转化的反应热相当小而且转化速度较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的观点“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”来研究。已知:
P4(s、白磷)+5O2(g)=P4O10(s);Δ H=-2983.2 KJ·mol-1
P(s、红磷) + 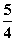 O2(g)=
O2(g)=  P4O10(s);Δ H=-738.5KJ·mol-1
P4O10(s);Δ H=-738.5KJ·mol-1
试写出白磷转化为红磷的热化学方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com