
��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ���ˮ��ƽ�����֣��Ҿ�������������ԭ������ش��������⣺
���ں����ܱ������У�������Ӧ3A(g)��B(g) 2C(g)����H��Q kJ/mol���ش��������⣺
2C(g)����H��Q kJ/mol���ش��������⣺
��1��д���÷�Ӧƽ�ⳣ���ı���ʽ__________��
��2�����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������________(�����)��
�� v(A)��3v(B) �ڻ��������ܶȱ��ֲ��䡡
����3 mol A���ĵ�ͬʱ��1 mol B���ɡ� ��C��Ũ�ȱ��ֲ���
��3������ʵ���õ����ݿ�֪���¶�Խ�߸÷�Ӧ�Ļ�ѧƽ�ⳣ��Խ����Q______0(����ڡ���С�ڡ�)��
��1�������£�ȡpH��2������ʹ�����Һ��100 mL�������зֱ����������Zn������Ӧ����������Һ��pH�仯��ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ���________(�� ��a����b��)���������м���Zn����Ϊm1��������Һ�м����Zn����Ϊm2����m1________m2(ѡ�����������������)��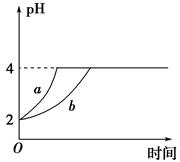
��2����������pH��2������ʹ�����Һ�� 100 mL���ֱ��ˮϡ�ͺ�ʹpH��4���������м���ˮ�����ΪV1��������Һ�м����ˮ�����ΪV2���� V1______V2(���������������)��
�����£�Ũ�Ⱦ�Ϊ0.1 mol/L ������������Һ��pH���±���
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
��.��K=c2��C��/c3��B��c��A���� �ۢ� �Ǵ��ڡ�
��.(1) b���� �� ��(2) �� ��
��.�� CO32 �� ���� D �� C �� �� C ��
�� ��ȥZnCl2��xH2O�е�ˮ��ͬʱ����HCl������������ZnCl2��ˮ�� ��
���������������.�ŷ�Ӧ3A(g)��B(g) 2C(g)��ƽ�����ʽΪK=c2��C��/c3��B��c��A����
2C(g)��ƽ�����ʽΪK=c2��C��/c3��B��c��A����
��2�����÷�Ӧ�ﵽƽ��ʱ�� v(A)��3v(B)������Ϊ���־����Ϊ�������̶���v(A)��3v(B)�����������ܶȱ��ֲ��䣬������Ϊ��ﵽƽ��ı�־����Ϊ���������л��������ܶȱ��ֲ��䣻��3 mol A���ĵ�ͬʱ��1 mol B���ɺ�C��Ũ�ȱ��ֲ��������Ϊ�ж���ﵽƽ��ı�־�����Ա���Ĵ�Ϊ�ۢܣ�
��3���¶�Խ�߸÷�Ӧ�Ļ�ѧƽ�ⳣ��Խ������������ԭ��������֪���÷�ӦΪ���ȷ�Ӧ������Q����0��
��1��pH��2������ʹ��ᣬ��ͬ����������£���������ʵ���ԶԶ������������ʵ���������������п��Ӧʱ�����ڴ���ϵ���������ӣ����ԱȽ����ﵽpH=4������ͼ�б�ʾ������Һ��pH�仯���ߵ���b���Ҵ������ĵ�п�������ϴ�
��2��pH��2������ʹ��ᣬ��ͬ����������£���������ʵ���ԶԶ������������ʵ��������Լ�ˮϡ�ͺ�ʹpH��4����������ˮ������ϴ�
��1����������Һ�е������ӣ�pHԽ����˵�����H+������Խ�����Խ��H+������ǿ����CO32 �� ������Һ�е������ӣ�pHԽС��˵��������Խǿ������CH3COOH ��������ǿ��������ˮ�е��ܽ�Ⱥ�С�����Խ�����Һ�ֱ�ϡ��100���� pH�仯��С���DZ��ӣ���3������ǿ���Ʊ������ԭ��������֪��CO2��H2O��2C6H5 ONa��Na2CO3��2C6H5OH���ܹ���������Ϊ̼��������Աȱ��������ʲ��ﲻ�ܳ���Na2CO3�����Դ�ѡ��C��
����ΪSOCl2 (�Ȼ�����)����ˮ�������·�Ӧ��SOCl2��H2O=SO2��2HCl��������HCl����������п���ӵ�ˮ�⣬�ҿ�������ZnCl2��xH2O�е�ˮ����SOCl2�������Ƕ�ȥZnCl2��xH2O�е�ˮ��ͬʱ����HCl������������ZnCl2��ˮ�⡣
���㣺��ѧƽ�⡢ǿ������ʡ�����ˮ��
�����������ۺϿ����˻�ѧƽ�⡢ǿ������ʡ�����ˮ������֪ʶ�������ۺ���ǿ���漰�ķ�Χ�ȽϹ㣬������һ�����Ѷȡ�


 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
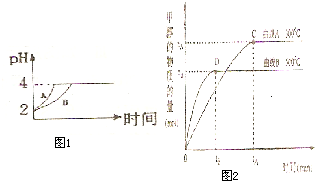 ��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺
��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺| c(CH3OH) |
| c(CO)��c2(H2) |
| c(CH3OH) |
| c(CO)��c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ѧѧ���е�ƽ��������Ҫ���ݰ�������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ������֣��Ҿ�������������ԭ������ش��������⣮
��ѧѧ���е�ƽ��������Ҫ���ݰ�������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ������֣��Ҿ�������������ԭ������ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺
��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| O | 2- 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
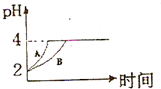 ��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺�����£�ȡ pH=2������ʹ�����Һ��100mL�������зֱ����������Zn������Ӧ����������Һ��pH�仯��ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ���
��ѧѧ���е�ƽ��������Ҫ��������ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ�����֣��Ҿ�������������ԭ������ش��������⣺�����£�ȡ pH=2������ʹ�����Һ��100mL�������зֱ����������Zn������Ӧ����������Һ��pH�仯��ͼ��ʾ����ͼ�б�ʾ������Һ��pH�仯���ߵ����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com