
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 浓硫酸 |
| 浓硫酸 |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013届新课标高三配套月考(四)化学试卷(A卷)(带解析) 题型:实验题
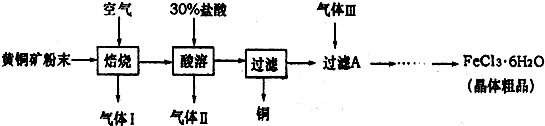
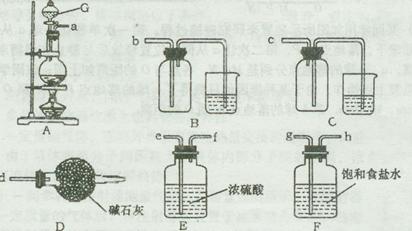
[2012·潍坊一模] (14分)黄铜矿的主要成分是CuFeS2,是工业炼铜的主要原料。已知黄铜矿在空气中焙烧生成Cu、FeS和SO2,FeS+2HCl=FeCl2+H2S↑,H2S是一种剧毒气体。某科研小组设计以黄铜矿为原料制取单质铜和氯化铁晶体(FeCl3·6H2O)的流程如下:

(1)92gCuFeS2在空气中焙烧生成Cu、FeS和SO2转移电子的物质的量为 。
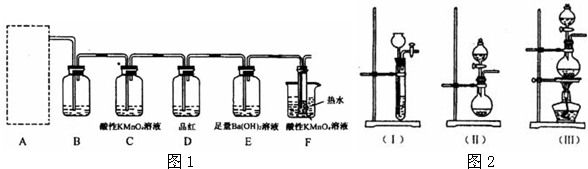
(2)请简述检验气体Ⅰ的操作步骤 。
(3)在实验室中,欲用38%(密度为1.18g·mL-1)的盐酸配制30%的盐酸,需要的玻璃仪器主要有 。
(4)气体Ⅲ最好选用 (填写序号),其主要作用是 。
| A.O2 | B.H2 | C.Cl2 | D.N2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年新课标高三配套月考(四)化学试卷(A卷)(解析版) 题型:实验题
[2012·潍坊一模] (14分)黄铜矿的主要成分是CuFeS2,是工业炼铜的主要原料。已知黄铜矿在空气中焙烧生成Cu、FeS和SO2,FeS+2HCl=FeCl2+H2S↑,H2S是一种剧毒气体。某科研小组设计以黄铜矿为原料制取单质铜和氯化铁晶体(FeCl3·6H2O)的流程如下:

(1)92gCuFeS2在空气中焙烧生成Cu、FeS和SO2转移电子的物质的量为 。
(2)请简述检验气体Ⅰ的操作步骤 。
(3)在实验室中,欲用38%(密度为1.18g·mL-1)的盐酸配制30%的盐酸,需要的玻璃仪器主要有 。
(4)气体Ⅲ最好选用 (填写序号),其主要作用是 。
A.O2 B.H2 C.Cl2 D.N2
欲选用下列仪器在实验室中制取纯净干燥的该气体。
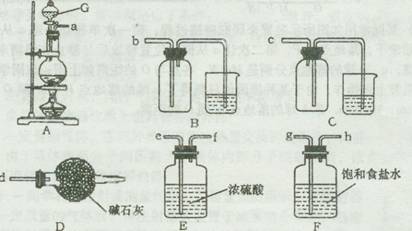
装置A中发生反应的离子方程式为 。
选用合适装置导管口的连接顺序为a接 。图中仪器G的名称是 ;在使用该仪器时,应首先 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com