
| A. | 22.4g | B. | 11.2g | C. | 5.6g | D. | 无法计算 |
分析 加入100ml 2mol/L的硫酸恰好使混合物完全溶解,硫酸没有剩余,向反应所得溶液加KSCN溶液无血红色出现,说明溶液为FeSO4溶液,根据S元素守恒可知n(FeSO4)=n(H2SO4);用足量的CO在高温下还原相同质量的混合物得到铁,根据铁元素守恒可知n(Fe)=n(FeSO4),此结合m=nM计算铁的质量.
解答 解:Fe、Fe2O3、Fe3O4的混合物中,加入100ml 2mol/L的硫酸,恰好使混合物完全溶解,所得溶液中加入KSCN溶液无血红色出现,说明反应后溶质为FeSO4,根据S元素守恒可知n(FeSO4)=n(H2SO4),
用足量的CO在高温下还原相同质量的混合物得到铁,根据铁元素守恒可知n(Fe)=n(FeSO4)=n(H2SO4)=2mol/L×0.1L=0.2mol,其质量为:56g/mol×0.2mol=11.2g,
故选B.
点评 本题考查混合物的计算,为高频考点,把握反应后溶质组成、原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
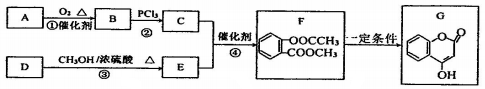
 +CH3COCl$\stackrel{催化剂}{→}$
+CH3COCl$\stackrel{催化剂}{→}$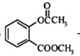 +HCl.
+HCl.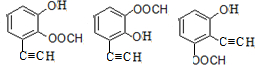 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
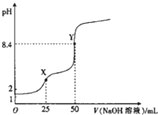 用0.1mot•L-1的NaOH溶液滴定25mL0.1mol•L-1 H2C2O4(草酸)溶液的滴定曲线如图所示,下列说法不正确的是( )
用0.1mot•L-1的NaOH溶液滴定25mL0.1mol•L-1 H2C2O4(草酸)溶液的滴定曲线如图所示,下列说法不正确的是( )| A. | 草酸是弱酸 | |
| B. | X点:c(H2C2O4)+c(HC2O4-)=c (Na+)-c(C2O42-) | |
| C. | Y 点:c(H2C2O4)+c(HC2O4-)=c(OH-)-C(H+) | |
| D. | 滴定过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 a L | B. | a L | C. | 2 a L | D. | 3 a L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
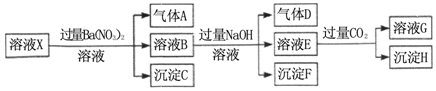
| A. | 溶液X中一定含有H+、Al3+、NH4+、Fe2+、SO42- | |
| B. | 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl- | |
| C. | 沉淀H为Al(OH)3、BaCO3的混合物 | |
| D. | 若溶液X为100mL,产生的气体A为44.8mL(标准状况),则X中c(Fe2+)=0.06mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 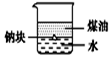 用图装置证明ρ(煤油)<ρ(钠)<ρ(水) | B. | 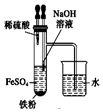 用图装置制备Fe(OH)2 | ||
| C. | 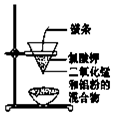 用图装置制取金属锰 | D. | 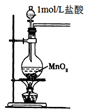 用图装置制取氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 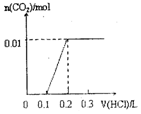 | B. | 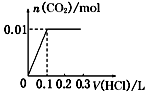 | C. | 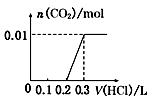 | D. | 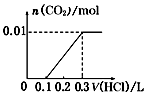 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
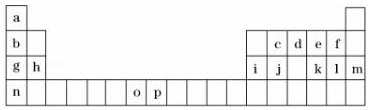
| 元素 | O | P | |
| 电离能/KJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com