
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
分析 (1)酸的电离平衡常数越大,其酸根离子水解程度越小,则相同浓度的钠盐溶液碱性越弱;
(2)NaCN和少量CO2反应生成NaHCO3、HCN;
(3)将0.02mol/L的HCN与0.01mol/L 的NaOH溶液等体积混合,溶液中的溶质是等物质的量浓度的NaCN、HCN,已知混合溶液中c(CN-)<c(Na+),根据电荷守恒可知c(H+)<c(OH-),混合溶液呈碱性,说明CN-的水解程度大于HCN的电离程度,据此进行判断;
(4)铝离子与碳酸氢根离子发生双水解反应生成二氧化碳气体和氢氧化铝沉淀;
(5)根据草酸氢铵溶液显示酸性及电荷守恒判断溶液中各离子浓度大小;根据电荷守恒写出草酸氢钠溶液中的电荷守恒表达式;
(6)根据化合价变化计算出生成4.48L二氧化碳转移的电子的物质的量.
解答 解:(1)电离平衡常数,CH3COOH>H2CO3>HCN,等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,故溶液的pH为:Na2CO3>NaCN>CH3COONa,
故答案为:b>a>c;
(2)NaCN和少量CO2反应生成NaHCO3、HCN,反应方程式为:NaCN+CO2+H2O=NaHCO3+HCN,
故答案为:NaCN+CO2+H2O=NaHCO3+HCN;
(3)将0.02mol/L的HCN与0.01mol/L 的NaOH溶液等体积混合,溶液中的溶质是物质的量浓度都为0.005mol•L-1的NaCN、HCN,测得c(Na+)>c(CN-),根据电荷守恒可知:c(H+)<c(OH-),溶液呈碱性,所以HCN的浓度为0.005mol•L-1,CN-的浓度小于0.005mol•L-1,
A.根据分析可知,溶液呈碱性,c(H+)<c(OH-),故A错误;
B.混合液呈碱性,则c(H+)<c(OH-),故B正确;
C.氢氧根离子浓度较小,c(CN-)远远大于c(OH-),故C错误;
D.根据物料守恒可知:c(HCN)+c(CN-)=0.01mol/L,故D正确;
故答案为:BD;
(4)铝离子与碳酸氢根离子混合发生双水解生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-═Al(OH)3↓+3CO2↑;
(5)草酸氢钠溶液显示酸性,则HC2O4-的电离程度大于其水解程度,所以c(C2O42-)>c(H2C2O4),由于氢离子来自水的电离和HC2O4-的电离,则c(H+)>c(C2O42-),HC2O4-的水解程度较小,则c(HC2O4-)>c(C2O42-),所以溶液中各离子浓度大小为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
草酸氢钠溶液中存在的电荷守恒为:c(OH-)+c(HC2O4-)+2c (C2O42-)=c(H+)+c(Na+),
故答案为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);c(OH-)+c(HC2O4-)+2c (C2O42-)=c(H+)+c(Na+);
(6)标准状况下4.48L二氧化碳的物质的量为:$\frac{4.48L}{22.4L/mol}$=0.2mol,H2C2O4中C元素的化合价为+3价,二氧化碳分子中C的化合价为+4价,则生成0.2mol二氧化碳转移的电子的物质的量为:0.2mol×(4-3)=0.2mol,
故答案为:0.2.
点评 本题考查了弱电解质的电离及其影响、离子浓度大小比较、原电池工作原理的应用等知识,题目难度中等,明确弱电解质的电离平衡及其影响因素、原电池工作原理为解答关键,试题知识点较多、综合性较强,充分考查了学生的灵活应用能力.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:填空题
 英国科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫因在石墨烯(如图)材料方面的卓越研究而获得2010年诺贝尔物理学奖.六方氮化硼(BN)与石墨是等电子体,它有“白石墨”之称,具有类似石墨的层状结构,有良好的润滑性.C、N、B的第一电离能由大到小的顺序为N>C>B,电负性由小到大的顺序为B<C<N.
英国科学家安德烈•海姆和康斯坦丁•诺沃肖洛夫因在石墨烯(如图)材料方面的卓越研究而获得2010年诺贝尔物理学奖.六方氮化硼(BN)与石墨是等电子体,它有“白石墨”之称,具有类似石墨的层状结构,有良好的润滑性.C、N、B的第一电离能由大到小的顺序为N>C>B,电负性由小到大的顺序为B<C<N.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol Na2O2与盐酸反应,转移的电子数为0.6NA | |
| B. | 2L 0.1mol/L Al2(SO4)3溶液中,Al3+的数目为0.4NA | |
| C. | 标准状况下,4.48L O2所含有的共用电子对数目为0.2NA | |
| D. | 在常温下,0.3mol NaHSO4固体中含有的离子数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与四氯化碳分子都是含有极性键的极性分子 | |
| B. | 甲烷与四氯化碳分子内的键角均为60° | |
| C. | 甲烷分子比四氯化碳稳定,因为C-H键键能比C-Cl键大 | |
| D. | 甲烷沸点低于四氯化碳,因为C-H键键长比C-Cl键短 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用氨水除去试管内壁上的银镜 | |
| B. | 用湿润的蓝色石蕊试纸检验氨气 | |
| C. | 硅酸钠溶液应保存在带玻璃塞的试剂瓶中 | |
| D. | 锌与稀硫酸反应时,要加快反应速率可滴加少量硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
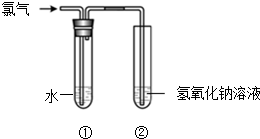 某同学用图所示装置制取氯水并进行相关实验.
某同学用图所示装置制取氯水并进行相关实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l) | B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l) | ||
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s) | D. | 2H2(g)+O2(g)═2H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
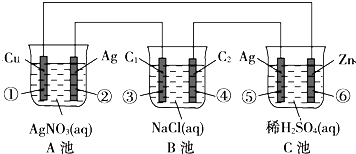
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com