
 2C��g��+ D��s�� ��5 min��ﵽƽ�⡣ƽ��ʱAΪ1.6mol���ų�������ΪQ����t0ʱ�̣�����ƽ����ϵ�з�����ķ�֮һ�Ļ�����壬��ƽ����ϵ��c(A)Ϊ0.6mol��L��
2C��g��+ D��s�� ��5 min��ﵽƽ�⡣ƽ��ʱAΪ1.6mol���ų�������ΪQ����t0ʱ�̣�����ƽ����ϵ�з�����ķ�֮һ�Ļ�����壬��ƽ����ϵ��c(A)Ϊ0.6mol��L��| ��ʼ n��A��/mol | ��ʼ n��B��/mol | ��ʼ n��C��/mol | ��ʼ n��D��/mol | �ﵽƽ��ʱ�ų��������գ������� |
| 0 | 1.6 | 8 | ���� | |
 2C��g��+ D��s��
2C��g��+ D��s��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


 ����ش��������⣺
����ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3C(g) ��H��0��ij�о�С���о���������������ʱ��ֻ�ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����( )
3C(g) ��H��0��ij�о�С���о���������������ʱ��ֻ�ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����( )
| A��ͼ���ʾ����t1ʱ�������¶ȶԷ�Ӧ���ʵ�Ӱ�� |
| B��ͼ���ʾ��һ����t1ʱ�̼��������Է�Ӧ���ʵ�Ӱ�� |
| C��ͼ���ʾ�����¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸ� |
| D��ͼ���ʾ���Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)���ݻ�Ϊ1L�����ܱ������зֱ����1molCO��2molH2��ʵ���ü״������ʵ������¶ȡ�ʱ��Ĺ�ϵ������ͼ��ʾ���������Ӧ�ġ�H_______0�����������������=�������жϵ�������______��
CH3OH(g)���ݻ�Ϊ1L�����ܱ������зֱ����1molCO��2molH2��ʵ���ü״������ʵ������¶ȡ�ʱ��Ĺ�ϵ������ͼ��ʾ���������Ӧ�ġ�H_______0�����������������=�������жϵ�������______��
 CH3OH+H2O��
CH3OH+H2O��

 CO(g)+2H2(g)�����ݻ�Ϊ2.0L���ܱ������г���0. 60 molCH3OH(g)����ϵѹǿΪP1����һ�������´ﵽƽ��ʱ����ϵѹǿΪP2����P2/P1 =2.2�����������CH3OH ��ƽ��ת����Ϊ______ ��
CO(g)+2H2(g)�����ݻ�Ϊ2.0L���ܱ������г���0. 60 molCH3OH(g)����ϵѹǿΪP1����һ�������´ﵽƽ��ʱ����ϵѹǿΪP2����P2/P1 =2.2�����������CH3OH ��ƽ��ת����Ϊ______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
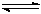 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)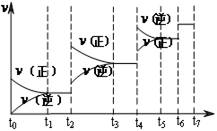
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

A������ͼ�ٿ��жϿ��淴ӦA2(g)+3B2(g) 2AB3(g)�Ħ�H��0 2AB3(g)�Ħ�H��0 |
B��ͼ�ڱ�ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g) 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�� 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�� |
| C��ͼ�ۿɱ�ʾ������Һ��ͨ�백����������������Һ�����Եı仯 |
| D������ͼ�ܣ�����ȥCuSO4��Һ�е�Fe3+�ɲ�������Һ�м�������CuO����pHԼΪ4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3(g) ��H=һ92. 4 KJ��mol-1
2NH3(g) ��H=һ92. 4 KJ��mol-1 N2(g) +3H2(g)�ں����ܱ������дﵽƽ��ı�־��
N2(g) +3H2(g)�ں����ܱ������дﵽƽ��ı�־��| A���٢ۢ� | B���٢ڢܢ� | C���٢ܢ� | D���ڢۢ� |
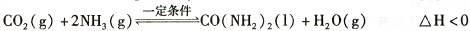
| ʱ�䣯min | ��0 | 30 | 70 | 80 | 100 |
| n(CO2) ��mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
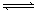 pC(g)+ qD(g)��������ͼʾ�ش�
pC(g)+ qD(g)��������ͼʾ�ش�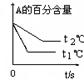
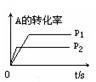
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OCH3(g)+H2O(g)��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£�������㶨���ܱ������м���һ������CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
CH3OCH3(g)+H2O(g)��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£�������㶨���ܱ������м���һ������CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/mol��L-1 | 0.44 | 0.6 | 0.6 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com