
����Ŀ���о���Ա������ú��������Ȼ�ѧѭ��ʵ��̫���ܵ�ת����洢���������£�
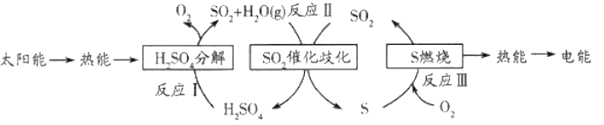
��ش��������⣺
��1����ҵ����H2SO4ʱ���һ����Ӧ�Ļ�ѧ����ʽ��_______________________��
��2����Ӧ��Ļ�ѧ����ʽ��_________________���������������뻹ԭ��������ʵ���֮����________________________��
��3����Ӧ��Ϊ�绯��Ӧ��������Ԫ�صĻ��ϼ�����____________��________________��
��4����Ӧ��������������ȼ��������________________________________���������ɵĶ�������ķ�����_________________________________________________���۲쵽��������_______________________________��
��5��������������__________����ʽ������ת�����˹����п������һ�ֻ���������_____________________________��
���𰸡�SO3+H2O��H2SO4 2H2SO4![]() 2SO2��+O2��+2H2O 1:2 +4 0��+6 ��������������ɫ���棬���ȣ������д̼�����ζ������ ������ͨ��Ʒ����Һ�У���һ����ټ��� Ʒ����Һ��ɫ���Ҽ��Ⱥ��ָֻ�ԭɫ 4 ����
2SO2��+O2��+2H2O 1:2 +4 0��+6 ��������������ɫ���棬���ȣ������д̼�����ζ������ ������ͨ��Ʒ����Һ�У���һ����ټ��� Ʒ����Һ��ɫ���Ҽ��Ⱥ��ָֻ�ԭɫ 4 ����
��������
��1����ҵ����H2SO4ʱ���һ����Ӧ�����������ˮ��Ӧ�������ᣬ�ݴ���д��
��2����Ӧ��������ֽ��������������������ˮ���ݴ���д������Ԫ�صĻ��ϼ۱仯���㣻
��3�����ݷ�Ӧ�������������Ԫ�صĻ��ϼ۷����жϣ�
��4��������ȼ�յ�ʵ��������������ö��������Ư���Լ��飻
��5������ת����ϵͼ�жϡ�
��1����ҵ����H2SO4ʱ���һ����Ӧ�����������ˮ��Ӧ�������ᣬ��Ӧ�Ļ�ѧ����ʽ��SO3+H2O=H2SO4��
��2����Ӧ��������ֽ��������������������ˮ����Ӧ�Ļ�ѧ����ʽ��2H2SO4![]() 2SO2��+O2��+2H2O����Ӧ����Ԫ�ػ��ϼ����ߣ����������������Ԫ�ػ��ϼ۽��ͣ�SO2�ǻ�ԭ������������������뻹ԭ�����������֮����1:2��
2SO2��+O2��+2H2O����Ӧ����Ԫ�ػ��ϼ����ߣ����������������Ԫ�ػ��ϼ۽��ͣ�SO2�ǻ�ԭ������������������뻹ԭ�����������֮����1:2��
��3����Ӧ��Ϊ�绯��Ӧ����������ת��Ϊ����͵��������������Ԫ�صĻ��ϼ�����+4�۵�+6�ۺ�0�ۡ�
��4����Ӧ�����������������ɶ�������ȼ�������Dz�������������ɫ���棬���ȣ������д̼�����ζ�����塣����������ʹƷ����Һ��ɫ����������ɵĶ�������ķ����ǽ�����ͨ��Ʒ����Һ�У���һ����ټ��ȣ��۲쵽��������Ʒ����Һ��ɫ���Ҽ��Ⱥ��ָֻ�ԭɫ��
��5������ʾ��ͼ��֪��̫����ת��Ϊ���ܣ�����ת��Ϊ��ѧ�ܣ���ѧ��ת��Ϊ���ܣ�����ת��Ϊ���ܣ���������������4����ʽ������ת���������ж��������������˹����п�����ɵ�һ�ֻ������������ꡣ



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ת�������������������ԭ������(����)
A. NO2��HNO3��NO B. ![]() ��NH3
��NH3
C. NH3��NO D. P2O5��H3PO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л���ṹ������˵����ȷ���� (�� ��)
A. ��ϩ�Ľṹ��ʽΪCH2CH2
B. ����������1molCH4��3molCl2��Ӧ���Ƶ�1molCHCl3
C. 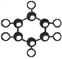 Ϊ�����ӵı���ģ��
Ϊ�����ӵı���ģ��
D. ![]() ������̼ԭ���п��ܶ���ͬһ��ƽ����
������̼ԭ���п��ܶ���ͬһ��ƽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ��������ԭ�Ϻϳɻ�״��E�߷��ӻ�����H��ʾ��ͼ������ʾ:
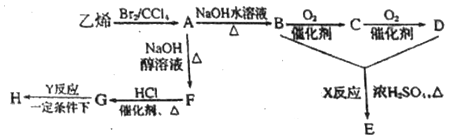
��ش���������:
��1��д���������ʵĽṹ��ʽ:A____________��H_____________��C�Ļ�ѧ����_____________��
��2��д�����·�Ӧ�ķ�Ӧ����:X_____________��Y_______________��
��3��д�����·�Ӧ�Ļ�ѧ����ʽ:
A��B:___________________________________________��
G��H:_________________________________��
B+D��E:________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ȥ����CO2�е�SO2��O2�������Լ���ʹ��˳����ȷ����(����)
�ٱ���Na2CO3��Һ���ڱ���NaHCO3��Һ
��ŨH2SO4��Һ�������ȵ�ͭ�����ݼ�ʯ��
A.�٢ۢ�B.�ڢۢ�
C.�ڢܢ�D.�ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪��N2��g��+3H2��g��![]() 2NH3��g����H=��92.4 kJ
2NH3��g����H=��92.4 kJ![]() ��
��
2H2��g��+O2��g��====2H2O��l����H=��571.6 kJ![]() ��
��
��2N2��g��+6H2O��l��![]() 4NH3��g��+3O2��g�� ��H=_______��
4NH3��g��+3O2��g�� ��H=_______��
��2��20����30�����Eyring��Pelzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ������������̬������ͼ����Ϣ���ش��������⣺
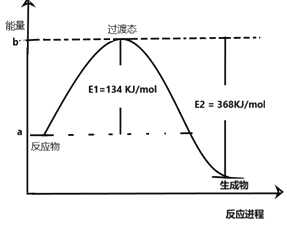
��ͼ��NO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��CO2��NO��Ӧ����NO2��CO���Ȼ�ѧ����ʽ��__________________________________���ڷ�Ӧ��ϵ�м��������E1��E2�ı仯�ǣ�E1__��E2__����������������С�����������������Է�Ӧ���Ƿ���Ӱ�죿__(��ǡ�����ԭ����________________________________________��
��3�����³�ѹ�¶���1 mol������ӻ�ѧ�������յ��������γ�1 mol������ӻ�ѧ�����ų���������Ϊ����(��λΪkJ��mol��1)���±���һЩ��������(kJ��mol��1)��������������⡣
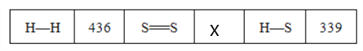
�Ȼ�ѧ����ʽ2H2(g)��S2(g)===2H2S(g)����H����229 kJ��mol��1����X��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ�������������ʷ�Ӧʱ�����ἴ����Ҳ�����ԣ��ֱ��ֳ����Ե��� �� ��
A. Cu(OH)2 B. Cu C. ľ̿ D. Fe2O3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڼ�����Һ���ܴ�����������ҺΪ��ɫ�����������ǣ� ��
A.K+ ��MnO4����Na+��Cl��B.K+��Na+��NO3����CO32��
C.Na+��H+��NO3����SO42��D.Al3+��Na+��Cl����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���AΪ��ɫӫ�⵰����һ��������ˮ������ղ���֮һ���ṹ��ʽΪ
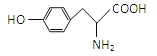
��ش��������⣺
��1������A�������ƶϴ������______��
a��A���ܺ��ᷴӦ���ܺͼӦ b��A���ܷ����ӳɷ�Ӧ
c��A���Է���������Ӧ d��A����ͨ�����۷�Ӧ�õ��߷��ӻ�����
��2��A������������Һ��Ӧ�Ļ�ѧ����ʽΪ______________��
��3����������4������A��ͬ���칹�������֣�д������һ��A��ͬ���칹��Ľṹ��ʽ________________________��
�� 1,3,5-��ȡ�������� ������������Һ����ɫ���� �����뱽��ֱ�������� �� ��������.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com