
| A. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 | |
| B. | 在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物(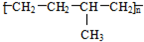 )可由单体CH3CH=CH2和CH2=CH2加聚制得 )可由单体CH3CH=CH2和CH2=CH2加聚制得 |
分析 A.己烷有五种同分异构体;
B.有机物分子中的原子或原子团被其它原子或原子团所取代的反应为取代反应;
C.油脂在碱性条件下水解生成甘油和高级脂肪酸盐;
D.凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可.
解答 解:A.己烷有五种同分异构体,其碳链结构分别为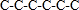 、
、 、
、 、
、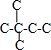 、
、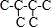 ,己烷同分异构体为不同物质,所以其熔沸点不同,且含有支链越多其熔沸点越低,故A错误;
,己烷同分异构体为不同物质,所以其熔沸点不同,且含有支链越多其熔沸点越低,故A错误;
B.在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应,是苯中的氢原子被溴原子、硝基、磺基取代,所以都属于取代反应,故B正确;
C.油脂水解生成高级脂肪酸和甘油,碱性条件下,高级脂肪酸和碱反应生成高级脂肪酸盐和水,所以实际上是油脂在碱性条件下水解生成甘油和高级脂肪酸盐,该反应为皂化反应,故C正确;
D.凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可,所以聚合物(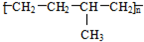 )的单体是CH3CH=CH2和CH2=CH2,故D正确;
)的单体是CH3CH=CH2和CH2=CH2,故D正确;
故选A.
点评 本题考查较综合,涉及高聚物单体判断、取代反应判断、同分异构体种类判断、油脂水解等知识点,侧重考查基本概念、基本理论,这些都是高频考点,难点是同分异构体种类判断,要考虑官能团异构、官能团位置结构、碳链异构,易错选项是D.


科目:高中化学 来源: 题型:解答题



查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
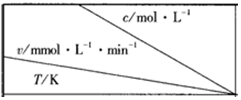 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a=6.00 | |
| B. | 同时改变反应温度和蔗糖的浓度,v可能不变 | |
| C. | b<318.2 | |
| D. | 不同温度时,蔗糖浓度减少一半所需的时间相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用LiOH和钴氧化物可制备锂离子电池正极材料.LiOH可由电解法制备,钴氧化物可通过处理钴渣获得.
利用LiOH和钴氧化物可制备锂离子电池正极材料.LiOH可由电解法制备,钴氧化物可通过处理钴渣获得.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=c(Na+)+c(H+) | |
| B. | 该溶液中的c(OH-)=1.0×10-3mol•L-1 | |
| C. | 加水稀释104倍所得溶液显碱性 | |
| D. | 与pH=3的HF溶液等体积混合所得溶液:c(Na+)=c(F-)+c(HF) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
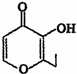 俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A. | lmol该有机物最多能与2molH2发生加成反应 | |
| B. | 该有机物能发生取代、加成和氧化反应 | |
| C. | 该有机物的分子式为C7H6O3 | |
| D. | 该有机物的一种芳香族同分异构体能发生银镜反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com