
【题目】图①和图②分别是1s电子的概率密度分布图和电子云轮廓图。下列认识正确的是( )

A.图①中的每个小黑点表示1个电子
B.图②表明1s电子云呈球形,有无数条对称轴
C.图②表示1s电子只能在球体内出现
D.不同能层的s电子云的半径相等
【答案】B
【解析】
电子的概率密度分布图是用小黑点形象地描述电子在原子核外空间各处出现的概率;电子云轮廓图是按某一标准(如出现概率为90%)将空间圈出来形成的图形。
A. 1s能级只有1个原子轨道,最多排2个电子,所以图①中的每个小黑点表示1个电子是错误的,小黑点的作用是通过其疏密来形象地描述电子在原子核外空间各处出现的概率,A选项错误;
B. 由图②可知,1s电子云轮廓图呈球形,球形对称图形有无数条对称轴,B选项正确;
C. 1s电子电子云轮廓图为球形,代表1s电子出现概率大的区域呈球形对称,但1s电子也可能在其它区域出现,只是出现的概率小,C选项错误;
D. 能层越大,s电子云的半径越大,D选项错误;
答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题。
(1)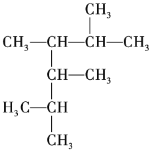 的名称为______。
的名称为______。
(2)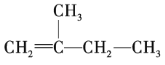 的名称为______。
的名称为______。
(3)3-甲基-2-戊烯的结构简式为______。
(4)1,3,5-三甲基苯的结构简式为______。
(5)某烷烃的相对分子质量为72,其一氯代物只有一种,该烷烃的结构简式为______。
(6)2,3-二甲基-2-丁烯的键线式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示,如:CH3-CH=CH-CH3可表示为![]() ,有一种有机物X键线式为
,有一种有机物X键线式为![]() 下列关于有机物X的叙述错误的是
下列关于有机物X的叙述错误的是![]()
A. X的分子式为C8H8O3
B. 有机物Y足X的同分异构体,含有苯环、能与NaHC03溶液反应、且有三个取代基,则Y的结构有8种
C. X分子中的所有原子不可能在同一平面内
D. X能发生加成反应,取代反应,并能使溴水、酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示,下列说法正确的是
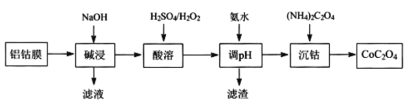
A.酸溶时H2O2做氧化剂,且温度不宜过高
B.加氨水调pH的目的是除铝
C.沉钴的离子方程式为:Co2++C2O42-=CoC2O4↓
D.在空气中加热4.41gCoC2O4得到钴的氧化物2.41g,则该氧化物的化学式为Co3O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F的原子序数依次增大;A、B的阴离子与C、D的阳离子的电子排布式均为1s22s22p6,A原子核外有2个未成对电子,且无空轨道,C单质可与热水反应但很难与冷水反应;E、F原子在基态时填充电子的轨道数为9,且E原子核外有3个未成对电子,F能与A形成相同价态的阴离子,且A离子半径小于F离子。
(1)上述六种元素中,第一电离能最大的是__(填元素符号),理由是__。
(2)比较C、D元素的第一电离能:__>__(填元素符号),理由是__。
(3)题述六种元素的电负性由小到大的顺序为__。
(4)C、D、E、F元素形成的最高价氧化物是离子化合物的有__(填化学式,下同),是共价化合物的有__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“臭苏打”是硫化钠的俗名,又称臭碱,黄碱,硫化碱,具有臭味,硫化钠溶解于冷水,极易溶于热水,微溶于醇,是重要的化工产品。
(1)硫化钠水溶液具有臭味是S2-水解产生H2S造成的,用离子方程式解释_____________。
(2)Na2S具有较强的还原性,其水溶液在空气中会缓慢地氧化成硫代硫酸钠,写出化学方程式__________________________________。
(3)某学习小组设计实验探究金属硫化物的性质。
Ⅰ.探究Na2S的还原性
甲同学取少量硫化钠溶液于试管,滴加2滴酚酞溶液,再滴加溴水溶液,观察到溶液颜色变浅。
①酚酞的作用是____________;写出该实验的离子方程式____________________
②乙同学认为甲方案不严密。他设计方案:取少量硫化钠溶液于试管,滴加适量苯,再用长滴管加入溴水。加入“苯”的目的是_________________________
Ⅱ.探究氧化还原反应和沉淀反应的竞争
丙同学设计以下两组实验:
实验1、①在10 mL 2 mol·L-1FeCl3溶液中滴加2 mL 1 mol·L-1Na2S溶液,观察到有浅黄色沉淀生成,溶液黄色变浅。
②在10mL 2 mol·L-1Na2S溶液中滴加2mL1 mol·L-1FeCl3溶液。观察到先产生浅黄色固体,随后生成黑色固体,溶液黄色变无色。
实验2、在2 mol·L-1Na2S溶液中滴加少量AgNO3溶液,立即产生大量黑色沉淀,没有浅黄色沉淀。
实验1 中产生的浅黄色固体是_______(填化学式)。写出实验1 ②中产生黑色沉淀的离子方程式_____________;已知:氧化性有Ag+>Fe3+,实验2中,发生复分解反应,未发生氧化还原反应。
实验结论:若某一溶液中同时存在氧化还原反应和沉淀反应,则_________(填“氧化还原”或“生成更难溶物质”)反应将优先进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在催化剂、400℃时可实现氯的循环利用,下图是其能量关系图下列分析正确的是
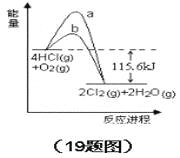
A. 曲线a是使用了催化剂的能量变化曲线
B. 反应物的总键能高于生成物的总键能
C. 反应的热化学方程式为:4HCl(g)+O2(g) = 2Cl2+2H2O(g)△H=-115.6 kJ
D. 若反应生成2mol液态水,放出的热量高于115.6kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mL浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释(溶液体积为V),溶液pH随lgV的变化情况如图所示,则下列说法正确的是( )
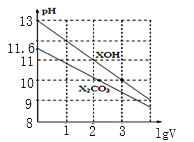
A.XOH是弱碱
B.pH=10的溶液中c(X+):XOH大于X2CO3
C.CO32-的水解常数Kh1约为1.0×10-3.8
D.当lgV=2时,升高X2CO3溶液温度,溶液碱性增强且![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】确定某液态有机物甲的结构简式的过程如下:
(1)测定甲的实验式:含C、H、O三种元素的有机物甲,经燃烧分析实验测得其所含碳元素的质量分数是64.86%,氢元素的质量分数是13.51%,则其实验式是__。
(2)确定甲的分子式:如图为有机物甲的质谱图,则其相对分子质量为__,分子式为__。
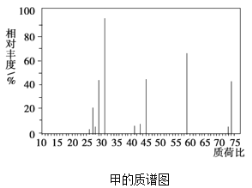
(3)确定甲的官能团:将小颗粒钠投入甲中,有气泡产生,则甲中存在的官能团的名称是__;甲可能的结构有__种。
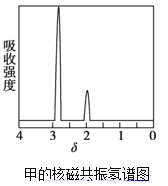
(4)确定甲的结构简式:经测定有机物甲的核磁共振氢谱如图所示,则甲的结构简式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com