
NA为阿伏加德罗常数,下列叙述正确的是( )
A.25℃时,l L pH=13的 Ba(OH)2 溶液中含有的OH-数为0.2 NA
B.18g D2O中含有的质子数为9NA
C.Fe在少量Cl2中燃烧生成0.5 mol 产物,转移的电子数为NA
D.标准状况下,11.2LCCl4含有的分子数为0.5 NA
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
将足量CO2通入下列各溶液中,所含离子还能大量共存的是( )
|
| A. | K+、SiO32﹣、Cl﹣、NO3﹣ | B. | H+、NH4+、Al3+、SO42﹣ |
|
| C. | Na+、S2﹣、OH﹣、SO42﹣ | D. | Na+、C6H5O﹣、CH3COO﹣、HCO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某可逆反应X(g)+Y(g)  Z(g)+2W(g),其化学平衡常数K和温度的关系如下表:
Z(g)+2W(g),其化学平衡常数K和温度的关系如下表:
| T/℃ | 700 | 800 | 850 | 1000 |
| K | 0.01 | 0.05 | 0.10 | 0.40 |
(1)上述反应的平衡常数表达式K=________,ΔH________0(填“>”或“<”)。加入催化剂,该反应的ΔH将________(填“增大”、“减小”或“不变”)。
(2)若上述反应在绝热恒容的密闭容器内进行,则能说明该反应达到化学平衡状态的依据有________。
A.混合气体的密度保持不变 B.v正(X)=v正(Z)
C.容器内温度恒定 D.W的质量分数不变
(3)在850 ℃、体积为1 L的密闭容器内,加入0.2 mol Z和0.3 mol W发生上述反应。X的c(X)-t曲线如图所示。
①0~4 min内W的平均速率为________mol·L-1·min-1。
②在5 min末将容器体积缩小至0.5 L,若在8 min末达到新平衡(此时X的浓度约为0.26 mol/L),请在图中画出5 min~9 min的X浓度的变化曲线。

查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质:①Cu ②KMnO4 ③氯化氢 ④CO2 ⑤NaHSO4
⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀盐酸
(1)属于电解质的有 (填选项)
A. ①②④⑨ B. ②③⑤⑥ C. ④⑤⑥⑧
(2)上述物质中有物质之间在水溶液中可发生离子反应:H++OH-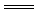 H2O,写出一个该离子反应对应的化学方程式 。
H2O,写出一个该离子反应对应的化学方程式 。
(3)②与⑨发生反应的化学方程式为: 2KMnO4 + 16HCl ══ 2KCl+2MnCl2+5Cl2↑+ 8H2O
上述反应的离子方程式 。标况下生成3.36LCl2,转移电子的数目为 ,被还原的盐酸的物质的量为 。
(4)向⑧中通入③至恰好完全反应,则⑧的导电能力的变化为
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组设计电解饱和食盐水的装置如下图,通电后两极均有气泡产生,下列叙述正确的是( )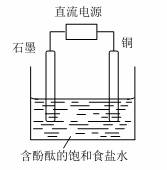
A.铜电极附近观察到黄绿色气体 B.石墨电极附近溶液先变红
C.溶液中的Na+向石墨电极移动 D.铜电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:A为淡黄色固体,E、X常温下为气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
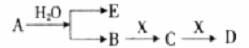
请回答下列问题:
(1)B中所含化学键的类型是______________。
(2)常温常压下,7.8g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式 。
(3)①C也可转化为B,写出该转化的化学方程式_______________。
②B与D反应的离子方程式为__________________________。
(4)将一定量的气体X通入2L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。
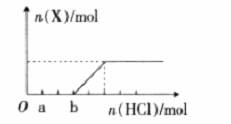
请回答:a 点溶液中所含溶质的化学式为__________,b 点溶液中各离子浓度由大到小的关系是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂鉴别正己烷、1﹣己烯、乙醇、苯酚水溶液4种无色液体,应选用( )
A.酸性KMnO4溶液 B.饱和溴水
C.NaOH溶液 D.AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,甲容器中的NH3和乙容器中的CH4所含的原子总数相同,则甲容器与乙容器的体积之比为( )
|
| A. | 1:1 | B. | 2:1 | C. | 3:4 | D. | 5:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com