
����Ŀ����������������ɴ�����Ⱦ����Ҫ���ʡ��о���������ķ�Ӧ������������������Ⱦ����Ҫ���塣NO�ڿ����д������·�Ӧ��2NO(g)+ O2(g)![]() 2NO2(g) ��H��������Ӧ��������ɣ���ͼ��ʾ��
2NO2(g) ��H��������Ӧ��������ɣ���ͼ��ʾ��

�ش��������⣺
��1��д����Ӧ�ٵ��Ȼ�ѧ����ʽ(��H�ú�������E�ĵ�ʽ��ʾ)��___________��
��2����Ӧ�ٺͷ�Ӧ���У�һ���ǿ췴Ӧ������ٽ���ƽ��״̬������һ��������Ӧ������2NO(g)+O2(g)![]() 2NO2(g)��Ӧ���ʵ���____(���Ӧ�١���Ӧ�ڡ�)���Ը÷�Ӧ��ϵ�����¶ȣ������ܷ�Ӧ���ʱ�������ԭ�������_________(��Ӧδʹ�ô���)��
2NO2(g)��Ӧ���ʵ���____(���Ӧ�١���Ӧ�ڡ�)���Ը÷�Ӧ��ϵ�����¶ȣ������ܷ�Ӧ���ʱ�������ԭ�������_________(��Ӧδʹ�ô���)��
��3��T1�¶�ʱ���ݻ�Ϊ2L�ĺ����ܱ�������ֻ����1.00molNO2���巢����Ӧ��2NO(g)+O2(g)![]() 2NO2(g)��ʵ���ã�v��=k��c2(NO)��c(O2)��v��=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO2)�����
2NO2(g)��ʵ���ã�v��=k��c2(NO)��c(O2)��v��=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO2)�����
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
�ٴ�0��2s�÷�Ӧ��ƽ������v(NO2)=___________mol/(L��s)��
��T1�¶�ʱ��ѧƽ�ⳣ��K=___________mol��1��L��
�ۻ�ѧƽ�ⳣ��K�����ʳ���![]() ��
��![]() ����ѧ��ϵ��K=___________�������������¶ȸı�ΪT2ʱ��
����ѧ��ϵ��K=___________�������������¶ȸı�ΪT2ʱ��![]() =
=![]() ����T1__________T2 (���������������=��)��
����T1__________T2 (���������������=��)��
(4)ˮ�ܲ�������NO��NO2�������õ�HNO2��Һ����20 mL 0.10 mol/LHNO2��Һ����μ���0.10 mol��L-1 NaOH��Һ������pH������ͼ��ʾ����A���Ӧ����Һ��![]() =_______��
=_______��

���𰸡�2NO(g) ![]() N2O2(g) ��H = -(E3-E4) kJ/ mol ��Ӧ�� �����ܷ�Ӧ���ʵ��Ƿ�Ӧ�ڣ��¶����ߺ�Ӧ��ƽ�������ƶ������N2O2Ũ�ȼ�С���¶����߶Է�Ӧ�ڵ�Ӱ������N2O2Ũ�ȼ�С��Ӱ�죬N2O2Ũ�ȼ�С���·�Ӧ�����ʱ��� 0.0875 8
N2O2(g) ��H = -(E3-E4) kJ/ mol ��Ӧ�� �����ܷ�Ӧ���ʵ��Ƿ�Ӧ�ڣ��¶����ߺ�Ӧ��ƽ�������ƶ������N2O2Ũ�ȼ�С���¶����߶Է�Ӧ�ڵ�Ӱ������N2O2Ũ�ȼ�С��Ӱ�죬N2O2Ũ�ȼ�С���·�Ӧ�����ʱ��� 0.0875 8 ![]() �� 10-3.70
�� 10-3.70
��������
(1)����ͼ�������Ӧ��Ϊ2NO(g)N2O2(g)���ʱ䣬д���Ȼ�ѧ����ʽ��
(2)����ͼ���֪����Ӧ�ٵĻ�ܣ���Ӧ�ڵĻ�ܣ���Ӧ��Ϊ�췴Ӧ����Ӧ��Ϊ����Ӧ�������÷�Ӧ���ʵ�������Ӧ����������Ӧ���ʵ��Ƿ�Ӧ�ڣ���������¶ȶԷ�Ӧ�ٺ͢ڵ�Ӱ��������ܵ�ԭ��
(3)�ٸ���v=![]() ��ϱ������ݼ��㣻�ڸ��ݱ������ݣ������ƽ��ʱ��c(NO2)��c(NO)��c(O2)���K=
��ϱ������ݼ��㣻�ڸ��ݱ������ݣ������ƽ��ʱ��c(NO2)��c(NO)��c(O2)���K= ���㣻��ƽ��ʱv��=v����������ʷ��̺ͻ�ѧƽ�ⳣ������ʽ�������㣻����ͼ�÷�Ӧ�Ƿ��ȷ�Ӧ�������������¶ȸı�ΪT2ʱ��
���㣻��ƽ��ʱv��=v����������ʷ��̺ͻ�ѧƽ�ⳣ������ʽ�������㣻����ͼ�÷�Ӧ�Ƿ��ȷ�Ӧ�������������¶ȸı�ΪT2ʱ��![]() =
=![]() ����K=1��8��˵��ƽ�������ƶ�������¶ȶ�ƽ���Ӱ������жϣ�
����K=1��8��˵��ƽ�������ƶ�������¶ȶ�ƽ���Ӱ������жϣ�
(4)����ͼ���֪��0.10molL-1HNO2��Һ��pH=2.15���ݴ˿ɼ����HNO2�ĵ���ƽ�ⳣ��Ka��A����ҺΪ���ԣ���c(H+)=c(OH-)=1��10-7mol/L����Һ�е���غ�Ϊc(H+)+c(Na+)=c(OH-)+c(NO2-)����A����Һ��c(Na+)=c(NO2-)��A���Ӧ����Һ�� =
=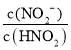 =
=![]() ���ݴ˼��㡣
���ݴ˼��㡣
(1)����ͼ���֪����Ӧ�ٵĻ�ѧ����ʽΪ��2NO(g)N2O2(g)��H=(E4-E3)kJ/mol=-(E3-E4) kJ/ mol���ʴ�Ϊ��2NO(g)N2O2(g)��H=-(E3-E4) kJ/ mol��
(2)����ͼ���֪����Ӧ�ٵĻ�ܣ���Ӧ�ڵĻ�ܣ���Ӧ��Ϊ�췴Ӧ����Ӧ��Ϊ����Ӧ������2NO(g)+O2(g)2NO2(g)��Ӧ���ʵ�������Ӧ�ڣ��Ը÷�Ӧ��ϵ�����¶ȣ������ܷ�Ӧ���ʱ��������ܵ�ԭ���ǣ������ܷ�Ӧ���ʵ��Ƿ�Ӧ�ڣ������¶Ⱥ�Ӧ��ƽ�������ƶ������N2O2Ũ�ȼ�С���¶����߶Է�Ӧ�ڵ�Ӱ������N2O2Ũ�ȼ�С��Ӱ�죬N2O2Ũ�ȼ�С���·�Ӧ�����ʱ������ʴ�Ϊ����Ӧ�ڣ������ܷ�Ӧ���ʵ��Ƿ�Ӧ�ڣ������¶Ⱥ�Ӧ��ƽ�������ƶ������N2O2Ũ�ȼ�С���¶����߶Է�Ӧ�ڵ�Ӱ������N2O2Ũ�ȼ�С��Ӱ�죬N2O2Ũ�ȼ�С���·�Ӧ�����ʱ�����
(3)�ٴ�0��2s�÷�Ӧ��ƽ������v(NO2)= = 0.0875mol/(L��s)���ʴ�Ϊ��0.0875��
= 0.0875mol/(L��s)���ʴ�Ϊ��0.0875��
�ڸ��ݱ������ݣ�ƽ��ʱ��c(NO2)=![]() =0.25mol/L����Ӧ�Ķ�������Ũ��c(NO2) =0.25mol/L������2NO(g)+O2(g)
=0.25mol/L����Ӧ�Ķ�������Ũ��c(NO2) =0.25mol/L������2NO(g)+O2(g)![]() 2NO2(g)��ƽ��ʱc(NO)= 0.25mol/L��c(O2) =0.125mol/L����T1�¶�ʱ��ѧƽ�ⳣ��K=
2NO2(g)��ƽ��ʱc(NO)= 0.25mol/L��c(O2) =0.125mol/L����T1�¶�ʱ��ѧƽ�ⳣ��K= =
=![]() =8mol��1��L���ʴ�Ϊ��8��
=8mol��1��L���ʴ�Ϊ��8��
��ƽ��ʱv��=v������k��c2(NO)��c(O2)=k��c2(NO2)����ѧƽ�ⳣ��K= =
=![]() �������������¶ȸı�ΪT2ʱ��
�������������¶ȸı�ΪT2ʱ��![]() =
=![]() ��K=1��8��˵��ƽ�������ƶ�����Ϊ�÷�Ӧ�Ƿ��ȷ�Ӧ��˵��T1��T2 ���ʴ�Ϊ��
��K=1��8��˵��ƽ�������ƶ�����Ϊ�÷�Ӧ�Ƿ��ȷ�Ӧ��˵��T1��T2 ���ʴ�Ϊ��![]() ������
������
(4)����ͼ���֪��0.10molL-1HNO2��Һ��pH=2.15����HNO2�ĵ���ƽ�ⳣ��Ka=![]() ��A����ҺΪ���ԣ���c(H+)=c(OH-)=1��10-7mol/L����Һ�е���غ�Ϊc(H+)+c(Na+)=c(OH-)+c(NO2-)����A����Һ��c(Na+)=c(NO2-)��A���Ӧ����Һ��
��A����ҺΪ���ԣ���c(H+)=c(OH-)=1��10-7mol/L����Һ�е���غ�Ϊc(H+)+c(Na+)=c(OH-)+c(NO2-)����A����Һ��c(Na+)=c(NO2-)��A���Ӧ����Һ�� =
=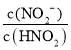 =
=![]() =
=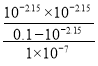 =103.70����
=103.70����![]() =10-3.70���ʴ�Ϊ��10-3.70��
=10-3.70���ʴ�Ϊ��10-3.70��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��387��ʱ,�ڼס������������Ϊ1.0L�ĺ����ܱ������з����״��ϳɶ����ѵķ�Ӧ��2CH3OH(g)![]() CH3OCH3(g) + H2O(g),��ʼʱ��ƽ��ʱ�����ʵ����ʵ������±���ʾ��
CH3OCH3(g) + H2O(g),��ʼʱ��ƽ��ʱ�����ʵ����ʵ������±���ʾ��
���� | ��ʼ���ʵ���/mol | ƽ�����ʵ���/mol | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | |
�� | 0.20 | 0.080 | 0.080 |
�� | 0.40 | a | a |
��1������a=________��
��2������ʼʱ��������г���0.20mol CH3OH(g)��0.50mol CH3OCH3��0.10molH2O(g)����Ӧ��ƽ��ʱ������CH3OH(g)��Ũ��Ϊ���٣�_______��д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в���Ԫ�ص�������ԭ��(�����)�ṹ�������Ϣ�����ʾ��
Ԫ�ر�� | Ԫ��������ԭ��(�����)�ṹ�������Ϣ |
T | �����������Ǵ����������� 3 �� |
X | �����µ��ʷ���Ϊ˫ԭ�ӷ��ӣ������к��� 3 �Թ��õ��Ӷ� |
Y | M ���K ���� 1 ������ |
Z | �������ǵ������ڽ���Ԫ�ص������а뾶��С�� |
(1)T��X��Y��Z �γɵļ����Ӱ뾶�ɴ�С��˳����_____��(�����ӷ��ű�ʾ)
(2)Ԫ�� Y ��Ԫ�� Z ��ȣ������Խ�ǿ����_____(��Ԫ�ط��ű�ʾ)�����б������� ֤����һ��ʵ����_____(����ĸ���)��
a.Y ���ʵ��۵�� Z ���ʵĵ�
b.Y �Ļ��ϼ۱�Z �ĵ�
c.������Y ������ˮ��Ӧ�ij̶Ⱥܾ��ң���Z �����ڼ��������²�����ˮ��Ӧ
d.Y ����������Ӧ��ˮ����ļ��Ա� Z ��ǿ
(3)T��X��Y��Z ��������Ԫ�����γɼȺ����Ӽ��ֺ��Ǽ��Թ��ۼ��ij��������д���û�����ĵ���ʽ��________��Ԫ�� X ����Ԫ����ԭ�Ӹ����� 1��2 �����γɳ����ڻ��ȼ�ϵĻ����� W��д�� W �ĵ���ʽ_______
(4)Ԫ�� T ����Ԫ����ԭ�Ӹ����� 1��1 �����γɻ����� Q�� Q ���� W ����������ԭ��Ӧ�� ����X �ĵ��ʺ�T ����һ���⻯�д���÷�Ӧ�Ļ�ѧ����ʽ��_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z ��ԭ�������������ӡ�m��p��r ������ЩԪ����ɵĶ�Ԫ�����n ��Ԫ��Z �ĵ��ʣ�ͨ��Ϊ����ɫ���壬q ��ˮ��Һ����Ư���ԣ�r ����ˮ��ǿ�ᣬs ͨ����������ˮ�Ļ����������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���� ( )

A.W �����ڱ���������ȫ�ǽ���B.X ������������ˮ����Ϊǿ��
C.Y ���⻯�ﳣ�³�ѹ��Ϊ��̬D.1molZ ����������������Һ��Ӧת�� 1mol ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��̽�� SO2 ���廹ԭ Fe3+������ʹ�õ�ҩƷ��װ����ͼ��ʾ������˵������������( )

A.Ϊ����֤ A �з�����������ԭ��Ӧ������KMnO4��Һ���Ϻ�ɫ��ȥ
B.Ϊ����֤ A �з�����������ԭ��Ӧ��������ϡ�����ữ��BaCl2��Һ��������ɫ����
C.�ܱ���I���Ļ�ԭ������SO2��������B����ɫ��Һ��ɫ
D.װ��C������������SO2β������ֹ��Ⱦ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ���г�����Һ���Լ������ữ�������ữ�����Ĵ�ʩ��ȷ����
A. ���Լ���SO![]() ����BaCl2��Һ��HNO3�ữ
����BaCl2��Һ��HNO3�ữ
B. Ϊ��߸��������Һ�����������������Ὣ���������Һ�ữ
C. ������Һ���Ƿ���Fe2��ʱ���������ữ
D. ������Һ���Ƿ���SO![]() ʱ���������������Ӹ��ŵ������£����������ữ��������Һ�ټ�BaCl2��Һ
ʱ���������������Ӹ��ŵ������£����������ữ��������Һ�ټ�BaCl2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z ��ԭ�������������ӡ�m��p��r ������ЩԪ����ɵĶ�Ԫ�����n ��Ԫ��Z �ĵ��ʣ�ͨ��Ϊ����ɫ���壬q ��ˮ��Һ����Ư���ԣ�r ����ˮ��ǿ�ᣬs ͨ����������ˮ�Ļ����������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���� ( )

A.W �����ڱ���������ȫ�ǽ���B.X ������������ˮ����Ϊǿ��
C.Y ���⻯�ﳣ�³�ѹ��Ϊ��̬D.1molZ ����������������Һ��Ӧת�� 1mol ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ģ�ҵ�Ʊ��ߴ������ö��Ե缫���FeSO4��Һ�Ʊ��ߴ�����ԭ������ͼ��ʾ������˵����ȷ���ǣ� ��

A. ������Ҫ������Ӧ��Fe2+ + 2e- =Fe
B. �����������μ�KSCN��Һ����Һ���
C. ���һ��ʱ�����������pH��С
D. ��ⷨ�Ʊ��ߴ����ܷ�Ӧ��3Fe2+![]() Fe + 2Fe3+
Fe + 2Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
��1��������Ԫ�����ڱ���ȫ���ǽ���Ԫ�ص�����Ϊ___��
A.a B.b C.c D.d
��2��GԪ����EԪ���γɵĻ�����Ļ�ѧʽ��___��___�����Ƕ���___�����������ۻ��������������ӻ����������������о���Ԫ�ص�����������Ӧ��ˮ�����У�������ǿ����___���û�����Ļ�ѧʽ��ʾ����ͬ����������ǿ����___���������������������___��
��3������Ԫ�ط��Ž���Ԫ����д������Ԫ�����ڱ��ж�Ӧ��λ��___��
��G��H��Ԫ����Ƚϣ������Խ�ǿ����___�������ƣ���������֤�ý��۵�ʵ����___�������ţ�
��a��������ԭ��ʧȥ�ĵ���Խ�࣬������Խǿ��
��b����������Ԫ�صĵ��ʷ�ĩ�ֱ��ͬŨ�ȵ����ᷴӦ
��c����������Ԫ�صĵ��ʷ�ĩ�ֱ����ˮ���ã��������̪��Һ
��d���Ƚ�������Ԫ�ص���̬�⻯����ȶ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com