
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | H-O | 464 |
| S=S | 255 | H-S | 339 | C-F | 427 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
分析 (1)由表中H-F的键能大于H-H,但F的半径大于H;
(2)由表中键能H-H>Cl-Cl,但Cl的非金属性大于H,由H-F、H-Cl、H-Br、H-I的键能分析与相同原子结合时,同主族元素形成的共价键,原子半径越小,共价键越强;
(3)Br的原子半径介于Cl与I之间,C-Br的键能介于C-Cl与C-I之间.
解答 解:(1))由表中数据可知,原子半径F>H,但键能:H-F>H-H,则不能得出半径越小的原子形成的共价键越牢固的结论,
故答案为:不能;
(2)Cl的非金属性大于H,但键能H-H>Cl-Cl,也不能说明非金属性越强的原子形成的共价键越牢固,由H-F、H-Cl、H-Br、H-I的键能可以看出,与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强,
故答案为:不能;与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强;
(3)Br的原子半径介于Cl与I之间,C-Br的键能介于C-Cl与C-I之间,即218KJ•mol-1~330 KJ•mol-1之间,
故答案为:218KJ•mol-1;330 KJ•mol-1.
点评 本题考查新信息数据处理能力,断裂化学键难易与形成化学键的两个原子的性质有关,比较时要选择同一标准,否则不可比,依题意,C-Br键能介于C-I、C-Cl键能之间,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+═2Fe3++3H2O | |
| B. | CaCO3与醋酸(CH3COOH)反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| C. | 向硫酸氢钾溶液中加入Ba(OH)2溶液至pH=7:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | MgSO4溶液跟Ba(OH)2溶液反应:SO42-+Ba2+=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
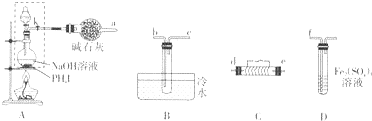
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO4>H2SO3 | B. | 氧化性:H2SO4(浓)>H2SO4(稀) | ||
| C. | 稳定性:CH4<SiH4 | D. | 碱性:Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
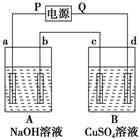 按图中装置实验,A、B两烧杯分别盛放200g 10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得电路通过电子0.5mol,试回答:
按图中装置实验,A、B两烧杯分别盛放200g 10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得电路通过电子0.5mol,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用于合成氨的工业煤气中含有H2S、C2H5SH(乙硫醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理.
用于合成氨的工业煤气中含有H2S、C2H5SH(乙硫醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CCl4可擦去圆珠笔油渍 | |
| B. | 蚊虫叮咬处涂抹肥皂水可止痛痒 | |
| C. | 煮鱼时加入少量食醋和料酒可除腥味,增加香味 | |
| D. | 小苏打可用作焙制面包 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
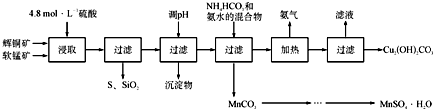
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn 2+ | 8.3 | 9.8 |
| Cu 2+ | 4.4 | 6.4 |
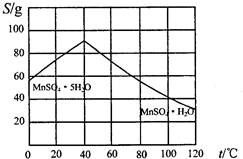
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com