
W”¢X”¢Y”¢ZŹĒĖÄÖÖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ĖęŌ×ÓŠņŹżµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ŅŃÖŖWµÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ18£¬ÖŠ×ÓŹżĪŖ10£»XŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠŌ×Ó°ė¾¶×ī“óµÄ£»YµÄµ„ÖŹŹĒŅ»ÖÖ³£¼ūµÄ°ėµ¼Ģå²ÄĮĻ£»ZµÄ·Ē½šŹōŠŌŌŚĶ¬ÖÜĘŚŌŖĖŲÖŠ×īĒ森ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
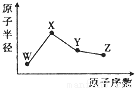
A£®¼ņµ„Ąė×Ó°ė¾¶£ŗW£¾X£¾Z
B£®×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗY£¼Z
C£®»ÆŗĻĪļXZWÖŠ¼Čŗ¬Ąė×Ó¼üÓÖŗ¬¹²¼Ū¼ü
D£®YµÄŃõ»ÆĪļÄÜÓėXµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·“Ó¦

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĞĻÄĮłÅĢÉ½ÖŠŃ§ø߶žÉĻµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¹ŲÓŚĒ攢Čõµē½āÖŹµÄŠšŹö£¬“ķĪóµÄŹĒ
A£®Ēæµē½āÖŹŌŚČÜŅŗÖŠĶźČ«µēĄė£¬²»“ęŌŚµēĄėĘ½ŗā
B£®ŌŚČÜŅŗÖŠ£¬µ¼µēÄÜĮ¦ĒæµÄµē½āÖŹŹĒĒæµē½āÖŹ£¬µ¼µēÄÜĮ¦ČõµÄµē½āÖŹŹĒČõµē½āÖŹ
C£®Ķ¬Ņ»Čõµē½āÖŹµÄČÜŅŗ£¬µ±ĪĀ¶Č”¢ÅØ¶Č²»Ķ¬Ź±£¬Ęäµ¼µēÄÜĮ¦Ņ²²»Ķ¬
D£®“æ¾»µÄĒæµē½āÖŹŌŚŅŗĢ¬Ź±£¬ÓŠµÄµ¼µē£¬ÓŠµÄ²»µ¼µē
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģ¹óÖŻŹŠøßČżÉĻѧʌµŚĖÄ“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
6.4gĶÓė¹żĮæµÄĻõĖį£Ø8mol/L£¬60mL£©³ä·Ö·“Ó¦ŗó£¬ĻõĖįµÄ»¹Ō²śĪļÓŠNO”¢NO2£¬·“Ó¦ŗóČÜŅŗÖŠĖłŗ¬H+Ąė×ÓĪŖnmol£¬“ĖŹ±ČÜŅŗÖŠĖłŗ¬NO3-µÄĪļÖŹµÄĮæĪŖ£ŗ
A£®0.28mol B£®0.3lmol C£®£Øn+0.2£©mol D£®£Øn+0.4£©mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģĮÉÄžŹ”øßČżÉĻѧʌ12ŌĀÄ£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČēĶ¼ŹĒŅŅ“¼Č¼ĮĻµē³ŲµÄŹµŃé×°ÖĆĶ¼£¬ĻĀĮŠÓŠ¹ŲĖµ·ØŅ»¶ØÕżČ·µÄŹĒ
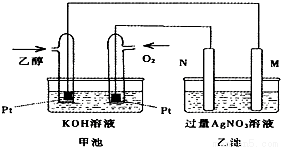
A£®ČōÓĆ“Ė×°ÖĆøųĢś°ōÉĻ¶ĘÉĻ²ćŅų£¬ŌņNµē¼«øÄÓĆĢśµē¼«£¬Mµē¼«øÄÓĆŅųµē¼«
B£®¼×³ŲÖŠøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗCH3CH2OH£12e-+3H2O=2CO2+12H+
C£®¼×³ŲKOHČÜŅŗÖŠ¾¹ż0.05molµē×ÓŹ±£¬ĄķĀŪÉĻŅŅ³ŲÖŠµÄMµē¼«ÖŹĮæŌö¼Ó5.40g
D£®Mµē¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ£ŗAg++e-=Ag
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÉĀĪ÷Ź”øßČżÉĻѧʌ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
ijČÜŅŗXŗ¬ÓŠH+”¢Al3+”¢NH4+”¢Fe2+”¢Fe3+”¢CO32-”¢SO32-”¢SO42-”¢Cl-”¢NO3-ÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£¬Č”øĆČÜŅŗ½ųŠŠŹµŃ飬ŹµŃéÄŚČŻŗĶĻą¹ŲŹż¾Ż£ØĘųĢåĢå»żŌŚ±ź×¼×“æöĻĀ²ā¶Ø£©ČēĻĀ£ŗ
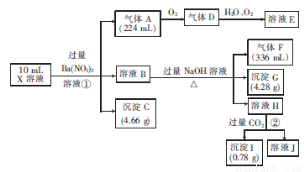
£Ø1£©ĶعżÉĻŹöŹµŃé¹ż³Ģ£¬Ņ»¶Ø²»“ęŌŚµÄĄė×ÓŹĒ________________________”£
£Ø2£©Š“³öÓŠ¹ŲĄė×Ó·½³ĢŹ½£ŗ²½Öč¢ŁÖŠÉś³ÉA________________________”£
£Ø3£©Čō²āµĆXČÜŅŗÖŠc(H+)=5 mol”¤L-1£¬ŌņXČÜŅŗÖŠ_______(Ģī”°ŗ¬”±»ņ”°²»ŗ¬”±)Fe3+£¬c(Fe3+)=______mol”¤L-1(ČōĢī²»ŗ¬£¬Ōņ²»Šč¼ĘĖć)£¬XČÜŅŗÖŠc(C1-)=____________ mol”¤L-1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÉĀĪ÷Ź”øßČżÉĻѧʌ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
2015Äź10ŌĀ5ČÕ£¬ÖŠ¹śÅ®Ņ©Ń§¼ŅĶĄßĻßĻÓėĮķĶāĮ½Ī»æĘѧ¼Ņ¹²Ļķ2015ÄźÅµ±“¶ūÉśĄķѧ»ņŅ½Ń§½±”£ĶĄßĻßĻŅņ·¢ĻÖŅ±ĮĘű¼²ŠĀŠĶŅ©ĪļĒąŻļĖŲŗĶĖ«ĒāĒąŻļĖŲ¶ų»ń½±”£ĒąŻļĖŲµÄ·Ö×ÓŹ½ĪŖC15H22O5”£ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ
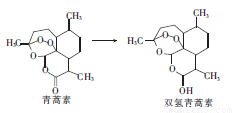
A£®ĒąŻļĖŲÖŠŃõŌŖĖŲµÄÖŹĮæĪŖ80g
B£®Ė«ĒāĒąŻļĖŲÄÜ·¢Éśõ„»Æ·“Ó¦
C£®Ė«ĒāĒąŻļĖŲÄÜÓėäåĖ®·¢Éś¼Ó³É·“Ó¦
D£®ĒąŻļĖŲŗĶĖ«ĒāĒąŻļĖŲ¾łŗ¬ōĒ»ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗž±±Ź”ĻåŃōŹŠĖÄŠ£øßŅ»ÉĻѧʌʌ֊ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĖĪ“śÖųĆū·ØŅ½Ń§¼ŅĖĪ“Č µÄ”¶Ļ“Ō©¼ÆĀ¼”·ÖŠÓŠ”°ŅųÕėŃ鶾”±µÄ¼ĒŌŲ£¬”°ŅųÕėŃ鶾”±µÄŌĄķŹĒ4Ag+2H2S+O2 = 2X+2H2O£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®XµÄ»ÆѧŹ½ĪŖAg2S B£®ŅųÕėŃ鶾Ź±£¬æÕĘųÖŠŃõĘųµĆµ½µē×Ó
 C£®·“Ó¦ÖŠAgŗĶH2S¾łŹĒ»¹Ō¼Į D£®ĆæÉś³É1mo1X£¬·“Ó¦×ŖŅĘ2mo1 e£
C£®·“Ó¦ÖŠAgŗĶH2S¾łŹĒ»¹Ō¼Į D£®ĆæÉś³É1mo1X£¬·“Ó¦×ŖŅĘ2mo1 e£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓ±±ŗŖµ¦ĪŗĻŲŅ»ÖŠ”¢ĒśÖÜĻŲŅ»ÖŠøßŅ»ÉĻĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ĢśŗĶĻ”ŃĪĖį·“Ó¦£ŗ2Fe + 6H+ = 2Fe3++3H2”ü
B£®Ģ¼ĖįÄĘÓėŃĪĖį·“Ó¦£ŗCO32-+2H+ = CO2”ü+H2O
C£®ĒāŃõ»Æ±µÓėĻ”ŃĪĖįµÄ·“Ó¦£ŗBa(OH)2+2H+ = Ba2++2H2O
D£®Ķʬ²åČėĻõĖįŅųČÜŅŗÖŠ£ŗCu+Ag+ = Cu2++Ag
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗž±±Ź”ŌęŃōŹŠøßŅ»ÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠÓŠ¹ŲŠšŹö²»ÕżČ·µÄŹĒ
A£® 1 molŅŅĶé·Ö×ÓÖŠŗ¬ÓŠ¹²¼Ū¼ü×ÜŹżĪŖ7NA
B£® 1 mol¼×»ł£Ø”ŖCH3£©Ėłŗ¬µÄµē×Ó×ÜŹżĪŖ9NA
C£® ±ź×¼×“æöĻĀ£¬22.4L±½ĶźČ«Č¼ÉÕŗÄŃõ·Ö×ÓŹżĪŖ8.5NA
D£® 1 mol¶”Ķé±»ĀČĘųĶźČ«Č”“śŹ±ĻūŗĵÄĀČ·Ö×ÓŹżĪŖ10NA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com