
����Ŀ��ʵ���Һϳ��屽��װ��ͼ���й��������£������кϳɲ���ش�
�� | �� | �屽 | |
�ܶ�/g��cm��3 | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
ˮ���ܽ�� | �� | �� | �� |

(1)ʵ��װ���У�����c������Ϊ__________________������Ϊ__________��
(2)��a�м���15 mL��ˮ����������м����b��С�ļ���4.0 mLҺ̬�壬��a�е��뼸���壬�а�������������Ϊ������________���壬�����μ���Һ����ꡣд��a�з�����Ӧ�Ļ�ѧ����ʽ��__________________��
(3)Һ�����������в�������ᴿ��
����a�м���10 mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����Һ������10 mLˮ��8 mL 10%��NaOH��Һ��10 mLˮϴ�ӡ�NaOH��Һϴ�ӵ�����__________��
����ֳ��Ĵ��屽�м�����������ˮ�Ȼ���(һ�ָ����)�����á����ˡ�������ˮ�Ȼ��Ƶ�Ŀ����__________________��
(4)�����Ϸ���������屽�л����е���Ҫ����Ϊ______��Ҫ��һ���ᴿ������еIJ�������Ϊ________��
���𰸡����������� �������� HBr 2Fe+3Br2=2FeBr3��![]() +Br2
+Br2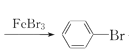 +HBr ��ȥδ��Ӧ��Br2 �����屽 �� ����
+HBr ��ȥδ��Ӧ��Br2 �����屽 �� ����
��������
���������ñ���Һ�������廯���������������£���������ƿ�ڷ���ȡ����Ӧ�Ʊ��屽����Ӧ������Ϊ��ֹҺ��ͱ��Ļӷ������ԭ�������ʣ��������ܽ�������������ͬʱ�������ɵ�HBr���壬�Է�ֹ������Ⱦ����Ӧ��Ļ����ͨ�����˳�ȥ��������ۣ�Ȼ��������������Һϴȥû�з�Ӧ���弰���ɵ�HBr������ˮ�Ȼ��Ƹ�����ٽ�����������ᴿ��
(1)���������ṹ��֪������c�����������ܣ�ʹ��װ�õ�Ŀ����ʹ�ӷ�����ͱ������������»ص���Ӧ�����ڣ����ԭ�������ʣ�
(2)����Һ�巢��ȡ����Ӧ�����屽��HBr����Ӧ����HBr������ˮ�����γɰ�����װ��a�з�����Ӧ�Ļ�ѧ����ʽΪ2Fe+3Br2=2FeBr3��![]() +Br2
+Br2 +HBr��
+HBr��
(3)�屽�ᴿ�ķ����ǣ�����ˮϴ���ѿ������ܽ���ˮ�У�Ȼ����˳�ȥδ��Ӧ����м���ڼ�NaOH��Һ��������Ӧ��2NaOH+Br2=NaBr+NaBrO+H2O��ʹδ��Ӧ��Br2���NaBr��NaBrO���뵽ˮ�У�
�ۼ���ˮ�Ȼ������������������ˮ�Ȼ��Ƶ������Ǹ����屽��
(4)�����������õ����屽����������δ��Ӧ�ı��������屽���ܣ������ߵķе㲻ͬ�������˵���ķе�ϵͣ����Բ�������ķ������з��롣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��N2(g)��3H2(g) ![]() 2NH3(g) ��H��0��2SO2(g)��O2(g)
2NH3(g) ��H��0��2SO2(g)��O2(g)![]() 2SO3(g) ��H��0����ش��������⣺
2SO3(g) ��H��0����ش��������⣺
(1)��Ӱ�컯ѧ��Ӧ���ʺͻ�ѧƽ������ط�����Ҫ������NH3��SO3�����ɣ�������Ӧ��ȡ�Ĵ�ʩ��_______��ʵ�������в�ȡ�Ĵ�ʩ��_________��
(2)�ںϳɰ��Ĺ�ҵ�����У�Ҫ���������Ŀ����__________�����ϳ�SO3�Ĺ����У�����Ҫ�����SO3��ԭ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��������ؾ����������ṹ�����������Ļ��ϼ۲���Ϊ0�ۣ�����Ϊ��2�ۡ���ͼΪ�������ؾ����һ������(��������С���ظ���Ԫ)��������˵����ȷ����(����)
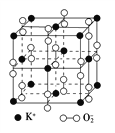
A. �������صĻ�ѧʽΪKO2��ÿ��������14��K����13��O
B. ������ÿ��K����Χ��8��O��ÿ��O��Χ��8��K��
C. ��������ÿ��K�����������K����8��
D. ������0����ԭ���룭2����ԭ�ӵ���Ŀ��Ϊ3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuCl����ʰ�ɫ���۵�Ϊ430�����е�Ϊ1490��������ֽ⣬¶���ڳ�ʪ�������ױ�������������ˮ��ϡ���ᡢ�Ҵ���������Ũ��������H3CuCl4����Ӧ�Ļ�ѧ����ʽΪCuCl��s��+3HCl��aq��H3CuCl4��aq����
��1��ʵ��������ͼ1��ʾװ����ȡCuCl����Ӧԭ��Ϊ��
2Cu2++SO2+8Cl��+2H2O�T2CuCl43��+SO![]() +4H+
+4H+
CuCl43����aq��CuCl��s��+3Cl����aq��
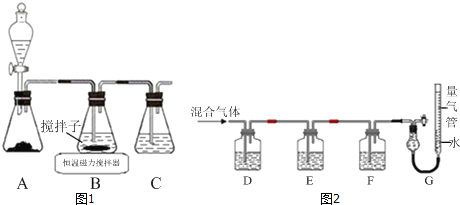
��װ��C��������_____��
��װ��B�з�Ӧ������ȡ������������ͼ��ʾ�������õ�CuCl���壮
�����![]()
![]()
![]()
![]()
![]() CuCl����
CuCl����
����������ҪĿ����_____
�����������ѡ�õ��Լ���_____��
��ʵ���ұ�������CuCl����ķ�����_____��
�����ᴿij����ͭ�۵�CuCl���壬�����ʵ�鷽����_____��
��2��ijͬѧ������ͼ2��ʾװ�ã��ⶨ��¯ú����CO��CO2��N2��O2�İٷ���ɣ�
��֪��
i��CuCl��������Һ������CO�γ�Cu��CO��ClH2O��
ii�����շۣ�Na2S2O4����KOH�Ļ����Һ������������
��D��Fϴ��ƿ����ʢ�ŵ��Լ��ֱ���_____��_____��
��д�����շۺ�KOH�Ļ����Һ����O2�����ӷ���ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
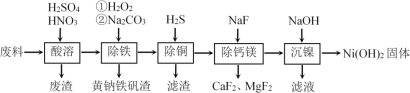
����Ŀ��һ�ִ��Բ��ϵ�ĥ�����ϣ�������������Լ21%����Ҫ�ɷ��������Ͻ𣬻�����ͭ���ơ�þ�����������ɸ÷����Ʊ����Ƚϸߵ����������������������£�
�ش��������⣺
��1���Ͻ��е���������ϡ���ᣬ�����ܡ�ʱ���˼���ϡ���ᣬ��Ҫ�߽����������ϡ���ᣬ��Ӧ��N2���ɡ�д���������ܽ�����ӷ���ʽ________________________��
��2����������ʱH2O2��������____________________��Ϊ��֤�����ӵ�H2O2��������Ӧѡ����Լ���____________________������軯�ء������軯�ء�����Һ����������[NaxFey(SO4)m(OH)n]���г��������������ʿ졢�����˵��ص㣬��x��y��m��n��1��3��2��________��
��3������ͭ��ʱ����Ӧ�����ӷ���ʽΪ_________________________������Na2S��Na2S2O3����H2S��ͭ���ŵ���__________________________��
��4����֪���ӹ������մ������н��У�NaF��ʵ������Ϊ����������1.1�����������˹����ԭ����_______________________________��
��5��100kg���Ͼ����������Ƶ�Ni(OH)2���������Ϊ31kg�����������ʵļ���ʽΪ_______��
��6���������ѳ�Ϊ��϶�����������Ҫ������ͣ��乤��ԭ�����£�M+Ni(OH)2![]() HM+NiOOH��ʽ��MΪ����Ͻ𣩡�д����طŵ�����������ĵ缫��Ӧʽ________��
HM+NiOOH��ʽ��MΪ����Ͻ𣩡�д����طŵ�����������ĵ缫��Ӧʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
1.����ƽF�ǽ�Ѫ֬�������̴���ҩ�����һ���ϳ�·�����£�

��1��AΪһԪ���ᣬ8.8g A������NaHCO3��Һ��Ӧ����2.24L CO2����״������A�ķ���ʽΪ_____________________________________________��
��2��д������A����ʽ�����м������Ľṹ��ʽ��_____________________��
��3��B���ȴ����ᣬ��˴Ź��������������壬д��B![]() C�ķ�Ӧ����ʽ��
C�ķ�Ӧ����ʽ��
__________________________________________________________��
��4��C+E![]() F�ķ�Ӧ����Ϊ________________________��
F�ķ�Ӧ����Ϊ________________________��
��5��д��A��F�Ľṹ��ʽ��
A______________________�� F__________________________��
��6��D�ı������������⣬�����������ŵ�����Ϊ___________________��д��a��b���������Լ���a ______________��b___________��
��.������·�ߣ���C�ɺϳɸ߾���H��
![]()
��7��C![]() G�ķ�Ӧ����Ϊ_____________________��
G�ķ�Ӧ����Ϊ_____________________��
��8��д��G![]() H�ķ�Ӧ����ʽ��_______________________��
H�ķ�Ӧ����ʽ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���㽭��ѧ�ɹ����Ƴ�����������֮�ڽ�����������Li-SOCl2��أ��õ�������������������ȵĵ����ɱ�ֻ�д�ͳ﮵�ص�һ�롣�����ҺΪLiAlCl4��SOCl2����ص��ܷ�ӦΪ��4Li+2SOCl2![]() 4LiCl+S+SO2������˵������ȷ����(����)
4LiCl+S+SO2������˵������ȷ����(����)
A.�ŵ�ʱ��������ӦʽΪ��Li �C e- = Li+
B.���øõ����Ϊ��ӵ�Դ���ͭ����������������64 gʱ�������Ͻ�����14g Li
C.�ŵ�ʱ�����Һ��Li+��Ǩ��
D.���ʱ��������ӦʽΪ��4Cl��+S+SO2��4e��=2SOCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᾧ�����ɿɱ�ʾΪH2C2O4��xH2O��ʵ���ҳ�������ȷֽ���ȡCO���壬��Ӧ����ʽΪ��H2C2O4��xH2O![]() CO��+CO2��+(x+1)H2O����ͼΪ�ֽ���ᾧ�壬�ø��﴿����CO��ԭCuO��ȡCu�����ռ�CO��ʵ��װ��(��ȥ����̨�����е�֧�żӳ�װ��)���ش��������⡣
CO��+CO2��+(x+1)H2O����ͼΪ�ֽ���ᾧ�壬�ø��﴿����CO��ԭCuO��ȡCu�����ռ�CO��ʵ��װ��(��ȥ����̨�����е�֧�żӳ�װ��)���ش��������⡣
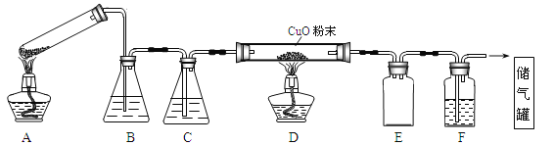
��1��ʵ��������漰�����²������ٵ�ȼA���ľƾ��� ��Ϩ��A���ľƾ��� �۵�ȼD���ľƾ��� ��Ϩ��D���ľƾ��ơ���ȼD���ƾ���ǰ����Ҫ���еIJ���������__________����4���������ȵ����˳��Ϊ______________(�����)��
��2��Aװ��Ϊ���ȷֽ�����װ�ã�ָ����װ��һ������_______________________��B��Fװ����ʢ�ŵ��Լ���ͬ������������__________ (�ѧʽ)��Eװ�õ�������__________��
��3�������Ը��������Һ�ζ����ᾧ�壬��x��ֵ��
ʵ�鲽�裺ȷ��ȡ1.08g ���ᾧ�壬���100mL��Һ��ȡ��20.00mL����ƿ�У�����ƿ�м�������ϡH2SO4����0.0500mol/L���Ը��������Һ�ζ����ζ����յ�ʱ���ĸ��������Һ16.00mL���ζ�ʱ���������ķ�ӦΪ��2MnO4��+5H2C2O4+6H+= 10 CO2��+2Mn2++8H2O��
�����Ʋ�����Һ����Ҫ��ͷ�ιܡ��ձ�����һ����Ҫ�IJ���������_____________��
��x=________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о���ѧϰС�����ʵ��̽��ͭ�ij�����ѧ���ʣ��������������ʾ
��������룩
����1�������ڱ��У�ͭ������λ�úܿ�����ͭ���������ã����������������ԡ���ô��������ͭҲ����������
����2������ͭ���б�ۣ�һ������£������������ȶ���С�������������ȶ��ԡ���ô����һ��ͭ���ȶ���ҲС��������ͭ���ȶ�����
����3������ͭ���������ԣ��ܱ�H2��CO��ԭ����ô������ͭҲ�ܱ�����ij����̬�⻯�ﻹԭ��
��ʵ��̽����
I���������1
��1�����õ���ҩƷ��1mol L-1 CuSO4��Һ��ϡ�����⣬����_________�����Լ��Ļ�ѧʽ����Һ��
��2���õ�����������1molL-1 CuSO4��Һ250mL��ѡ�õ��������ձ���������ƽ��ҩ�ס�����������ͷ�ιܡ������⣬����________�����������ƣ���
��3��Ϊ�ﵽʵ��Ŀ�ģ�����ΪӦ������Щ���ʵ�飿
ʵ�����ݺͲ��裺��_________����_______________��
�����������2
ȡһ�����Ƶõ�������ͭ���壬�����������գ����¶ȴﵽ80��100��ʱ�õ���ɫ�����ĩ������������1000�����ϣ���ɫ��ĩȫ����ɺ�ɫ��ĩ������ͭ��ȡ������ɫ������ͭ��ĩ�ڽ����Թ��У����������ϡ���ᣨ�����ᣩ���õ���ɫ��Һ��ͬʱ�۲쵽�Թܵײ����к�ɫ������ڡ���������ʵ������ش����⣺
��1��д��������ͭ��ϡ���ᣨ�����ᣩ��Ӧ�����ӷ���ʽ��_____________��
��2����ʵ�����ɵó��Ľ�����_______________________��
�����������3
�������װ�ã��г�װ��δ��������

������ij����̬�⻯�X������ͨ�����ȵ�����ͭʱ���۲쵽����ͭ�ɺ�ɫ����˺�ɫ����ˮCuSO4�������ɫ���������л���һ������Ⱦ�ĵ�������Y����Xͨ�����ȵ�CuOȼ�չ���ȫ��Ӧ������0.01molX�����Bװ������0.36g�����ռ���0.28g��������Y��
��1��X�����Ħ��������_________________��
��2��Cװ���з�����Ӧ�Ļ�ѧ����ʽΪ__________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com