
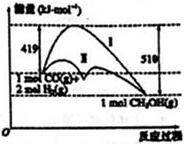
 已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )| A. | 反应物的总能量大于生成物的总能量 | |
| B. | 曲线Ⅰ和曲线Ⅱ相比较,曲线Ⅱ使用了催化剂 | |
| C. | 该反应可以表示为:CO(g)+2H2(g)?CH3OH(g)△=0.91KJ•mol-1 | |
| D. | 如果该反应生成液态CH3OH,则△H增大 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | - | ↓ | ↓ |
| C | - | - | - | ↓ | - | ↓ | ↓ |
| D | - | - | ↓ | - | ↓ | ↓ | ↓ |
| E | - | - | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电子由铁棒通过导线流向铜棒 | B. | 正极反应为Fe-2e-═Fe2+ | ||
| C. | 铜棒逐渐溶解 | D. | 该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用电解法精炼铜时,粗铜作阴极、精铜作阳极 | |
| B. | 在镀件上电镀铜时,用金属铜作阳极 | |
| C. | 在电解池中,铜作电极时,溶液中的阴离子在铜极上失电子 | |
| D. | 电解饱和食盐水制稀硫酸制Cl2、H2时,可用金属铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 $\stackrel{(1)O_{2}(2)Zn/H_{2}O}{→}$
$\stackrel{(1)O_{2}(2)Zn/H_{2}O}{→}$ +
+ (R1、R2、R3、R4为H或烷基)
(R1、R2、R3、R4为H或烷基)| A. | (CH3)2C=C(CH3)2 | B. |  | C. |  | D. | CH2=CH-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
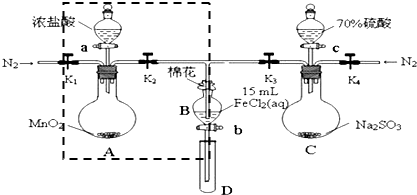
| 过程⑤B溶液中含有的离子 | 过程⑦B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
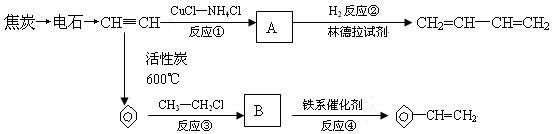
 .
. 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com