
【题目】火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会对环境造成严重影响。对燃煤废气进行脱硝脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。
利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ/mol
则甲烷直接将NO2还原为N2的热化学方程式为________________。
(2)脱碳。
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图所示,则上述CO2转化为甲醇的反应热△H3_____0(填“>”“<”或“=”),该反应的平衡常数表达式为_______________。
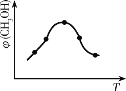
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图所示,试回答:
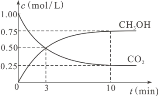
0~10 min内,氢气的平均反应速率为 ___________________mol/(L·min)。第10 min后,若向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数____________ (填“增大”“减小”或“不变”,下同),反应的平衡常数_____________________。
(3)脱硫。
①有学者想利用如图所示装置用原电池原理将SO2转化为重要的化工原料。AB是惰性电极,A极的电极反应式为:_________。
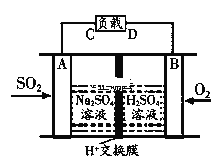
②某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。常温下,将NH4NO3 溶解于水中,为了使该溶液中的NH4+ 和 NO3-离子的物质的量浓度之比等于1 : 1,可以采取的正确措施为_________。
A.加入适量的硝酸,抑制 NH4+的水解
B.加入适量的氨水,使溶液的 PH = 7
C.加入适量的 NaOH 溶液,使溶液的PH = 7
D.加入适量的NH4NO3
【答案】CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=867kJ/mol < ![]() 0.225 变大 不变 SO22e+2H2O=4H++SO42 B
0.225 变大 不变 SO22e+2H2O=4H++SO42 B
【解析】
(1)依据热化学方程式和盖斯定律计算得到;
(2)①由图可知,到达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行;化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值;
②先根据图表,利用v=![]() 计算v(CO2),再利用各物质的反应速率之比等于计量数之比,确定v(H2);到达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行;化学平衡常数只受温度的影响;
计算v(CO2),再利用各物质的反应速率之比等于计量数之比,确定v(H2);到达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行;化学平衡常数只受温度的影响;
(3)①SO2与O2反应生成SO3,SO3再与水化合生成硫酸,根据硫酸的出口判断正负极,负极发生氧化反应,正极发生还原反应;
②硝酸铵是强酸弱碱盐,由于NH4+水解,因铵盐要发生水NH4++H2ONH3H2O+H+,导致溶液中c(NH4+)<c(NO3),根据加入的物质对铵根离子水解平衡的影响进行分析;
(1)①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=574kJmol1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=1160kJmol1
由盖斯定律(①+②)×![]() 得到CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=867kJ/mol,
得到CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=867kJ/mol,
故答案为:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=867kJ/mol;
(2)①由图可知最高点反应到达平衡,达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H3<0,化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,则化学平衡常数为K=![]() ,
,
故答案为:<;![]() ;
;
②由图可知,10min时,反应已经达平衡,△c(CO2)=1.00mol/L0.25mol/L=0.75mol/L,所以10min内,v(CO2)=![]() =0.075mol/(Lmin),反应速率之比等于计量数之比,故v(H2)=3v(CO2)=3×0.075mol/(Lmin)=0.225mol/(Lmin),第10min后,向该容器中再充入1molCO2和3molH2,等效为增大压强,平衡向正反应移动,CH3OH(g)的体积分数增大,化学平衡常数只受温度的影响,故化学平衡常数不变,
=0.075mol/(Lmin),反应速率之比等于计量数之比,故v(H2)=3v(CO2)=3×0.075mol/(Lmin)=0.225mol/(Lmin),第10min后,向该容器中再充入1molCO2和3molH2,等效为增大压强,平衡向正反应移动,CH3OH(g)的体积分数增大,化学平衡常数只受温度的影响,故化学平衡常数不变,
故答案为:0.225;变大;不变;
(3)①该原电池中,负极上失电子被氧化,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,则A为负极,A电极发生的反应为:SO22e+2H2O=4H++SO42,
故答案为:SO22e+2H2O=4H++SO42;
②硝酸铵是强酸弱碱盐,由于NH4+水解,因铵盐要发生水NH4++H2ONH3H2O+H+,导致溶液中c(NH4+)<c(NO3)。
A. 加入硝酸,氢离子的浓度增大能抑制铵根离子的水解,但硝酸中有硝酸根离子导致硝酸根离子的浓度增大,c(NH4+)<c(NO3),故A错误;
B. 加入氨水使溶液的PH=7,溶液中氢离子浓度等于氢氧根离子浓度,溶液呈中性,溶液中阴阳离子所带的电荷相等,所以c(NH4+):c(NO3)=l:l,故B正确;
C. 加入适量的NaOH,使溶液的pH=7,溶液中氢离子浓度等于氢氧根离子浓度,溶液呈中性,溶液中阴阳离子所带的电荷相等,[c(NH4+)+C(Na+)]:c(NO3)=l:l,所以c(NH4+):c(NO3)小于l:l,故C错误;
D. 再加入适量的NH4NO3,不能抑制铵根离子的水解,仍存在c(NH4+):c(NO3)小于l:l,故D错误;
故答案选B。


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:Ni(OH)2+5CH3NC=(CH3NC)4Ni+CH3NCO+H2O
(1)Ni2+基态核外电子排布式为________。
(2)CH3NC(其结构简式为CH3- N ![]() C)分子中碳原子轨道的杂化类型是_____;1molCH3NC中σ键的数目为_______。
C)分子中碳原子轨道的杂化类型是_____;1molCH3NC中σ键的数目为_______。
(3)用光气(COCl2)与甲胺(CH3NH2)可以制取CH3NCO。
①与COCl2互为等电子体的一种阴离子为___。
②甲胺极易溶于水,除因为它们都是极性分子外,还因为___。
(4)Ni单质的晶胞结构如下图所示,晶体中每个Ni原子周围与之距离最近的原子个数为______。
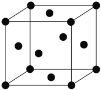
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4在实验室、生活、科学研究、工业生产中有广泛的应用。已知一种制备KMnO4的实验流程、原理及相关数据如下:

原理:反应I:3MnO2+KClO3+6KOH![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
反应Ⅱ:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
(墨绿色) (紫红色)
已知:25℃物质的溶解度g/100g水
K2CO3 | KHCO3 | KMnO4 |
111 | 33.7 | 6.34 |
(1)步骤②的副反应有少量单质气体生成,该反应的化学方程式为___________。
(2)步骤⑤中CO2______(填“能”或“不”能)过量,原因是_____________。
(3)流程中可循环利用的物质主要是_________(写化学式)。
(4)忽略本流程中含锰物质的循环利用,理论上0.3mol MnO2最多得到产品KMnO4的质量为________g。某同学在实验中得到干燥产品的质量多于理论值,排除称量因素,从步骤⑦分析,可能的原因是_______________。
(5)草酸钠滴定法分析高锰酸钾纯度步骤如下:
Ⅰ.称取1.5800g高锰酸钾产品,配成100mL溶液
Ⅱ.准确称取三份0.5360g已烘干的Na2C2O4,置于三个不同的洁净锥形瓶中,分别加入少量蒸馏水使其溶解,再加入少量硫酸酸化;
Ⅲ.锥形瓶中溶液加热到75~80℃,趁热用I中配制的高锰酸钾溶液滴定至终点。记录实验数据如表
实验次数 | V1(滴定前读数/mL) | V2(滴定后读数/mL) | (V2 -V1)/mL |
1 | 2.65 | 22.67 | 20.02 |
2 | 2.60 | 23.02 | 20.42 |
3 | 2.60 | 22.58 | 19.98 |
已知:2MnO4﹣+ 5C2O42﹣+16H+ =2Mn/span>2++ 10CO2↑+ 8H2O,则KMnO4的纯度为__________(保留四位有效数字);若滴定后俯视滴定管读数,所得KMnO4的纯度将___(填“偏高”或“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A. 断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应方程式对应且正确的是( )
A.氧化铁溶于氢碘酸:Fe2O3+6H+===2Fe3++3H2O
B.含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-===BaCO3↓+H2O
C.向氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=== AlO2-+4NH4++2H2O
D.向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O![]() CaSO3↓+2HClO
CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图的所示的转化关系。由此推断:
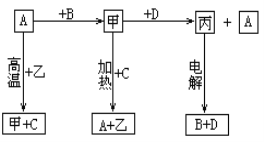
(1)甲的化学式为_____________,丙的化学式为______________。
(2)写出甲和D反应的化学方程式___________________________________________。
(3)为检验化合物甲中元素的化合价,需要用到的药品有_________________________。
A.稀硫酸 B.盐酸 C.硫氰化钾溶液 D.高锰酸钾溶液
(4)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:
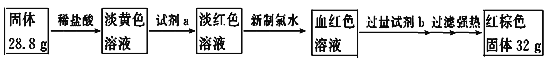
化合物甲的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气用途广泛,但在使用时,一般会产生氯化氢。工业上可用O2将HCl转化为Cl2,以提高效益,减少污染。反应为:O2+4HCl![]() 2Cl2 +2H2O。
2Cl2 +2H2O。
完成下列填空:
(1)该反应化学平衡常数K的表达式为___;实验测得P0压强下,HCl平衡转化率α(HCl)随反应温度T的变化如图所示,则正反应是___反应(填“吸热”或者“放热”)。
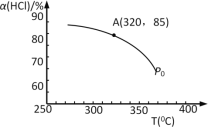
(2)上述实验中若压缩体积使压强由P0增大至P1,在图中画出P1压强下HCl平衡转化率α(HCl)随反应温度T变化的曲线___,并简要说明理由:___。
(3)该反应在P0、320℃条件下进行,达平衡状态A时,测得容器内n(Cl2)=7.2×10–3mol,则此时容器中的n(HCl)=___mol。
(4)对该反应达到平衡后,以下分析正确的是___(选填编号)。
a.增加n(HCl),对正反应的反应速率影响更大
b.体积不变加入稀有气体,对正反应的反应速率影响更大
c.压强不变加入稀有气体,对逆反应的反应速率影响更大
d.如果平衡常数K值增大,对逆反应的速率影响更大
(5)氯元素能形成多种离子。在水溶液中1molCl-、1molClOx–(x=1,2,3,4)能量的相对大小如图所示,写出B→A+C反应的化学方程式(用离子符号表示)___;若有1.5molB发生反应,转移电子___mol。
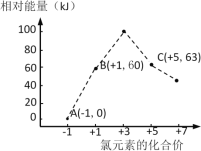
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 。
。
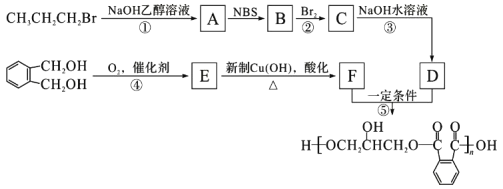
醇酸树脂是一种成膜性良好的树脂,下面是一种醇酸树脂的合成线路:
(1)B中含碳官能团的结构式为________,C的名称是_________。
(2)反应①的有机反应类型是 ________。
(3)下列说法正确的是____________(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2 mol Ag
b.F能与NaHCO3反应产生CO2
c.检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液。
(4)![]() 的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
a.能发生消去反应 b.能与过量浓溴水反应生成白色沉淀
(5)写出E与新制的氢氧化铜悬浊液反应的化学方程式_____________;
(6)写出反应⑤的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某饱和一元醇40.8g和足量金属Na反应,生成标准状况下氢气为4.48L,该醇可催化氧化生成醛的结构可能有( )
A.4种B.7种C.8种D.9种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com