
| A. | H3O+ | B. | H2O | C. | NO2+ | D. | NO2- |
分析 根据价层电子对互斥理论确定分子的空间构型及原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,据此分析解答.
解答 解:A.H3O+中O原子形成3个δ键,孤对电子数=$\frac{6-1-1×3}{2}$=1,为sp3杂化,立体构型为三角锥型,故A错误;
B.水分子中孤电子对数=$\frac{6-2×1}{2}$=2,水分子氧原子含有2个共价单键,所以价层电子对数是4,中心原子以sp3杂化轨道成键,价层电子对互斥模型为四面体型,含有2对孤对电子,分子的立体构型为V形,故B正确;
C.NO2+中N原子形成2个δ键,孤对电子数=$\frac{5-1-2×2}{2}$=0,中心原子为sp杂化,不含有孤电子对,离子的立体构型为直线形,故C错误;
D.NO2-中N原子形成2个δ键,孤对电子数=$\frac{5+1-2×2}{2}$=1,中心原子为sp2杂化,含有一个孤电子对,其空间构型是V形,故D正确;
故选BD.
点评 本题考查了微粒空间构型及原子杂化方式,根据价层电子对互斥理论来分析解答,难点的孤电子对个数的计算方法,为常考查点,要熟练掌握,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
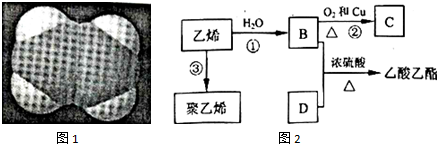
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃在任何情况下均不与强酸、强碱、氧化剂反应 | |
| B. | 正丁烷分子中四个碳原子可能在同一直线上 | |
| C. | 常温常压下 是气态 是气态 | |
| D. | 含有碳元素的化合物不一定是烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HI、H2、I2的浓度相等 | B. | HI、H2、I2的浓度不再发生变化 | ||
| C. | HI、H2、I2在密闭容器中共存 | D. | 反应停止,正、逆反应速率都等于零 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com