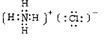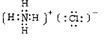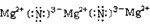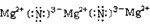(1)写出实验室制NH3的反应方程式为 ;
(2)硝酸具有强氧化性,它能和许多物质发生反应.写出浓硝酸与非金属单质碳的反应方程式. .
配平下列化学(或离子)方程式:
(3) FeCl2+ KNO3+ HCl- FeCl3+ KCl+ NO↑+ H2O
(4) SO32-+ MnO4-+ H+- Mn2++ SO42-+ H2O.
【答案】
分析:(1)根据实验室制NH
3的反应物和生成物写出相应的方程式;
(2)浓硝酸具有强氧化性,能和非金属单质C在加热条件下反应生成二氧化碳、二氧化氮和水,根据反应物、生成物写出相应的方程式;
(3)、(4)根据氧化还原反应中得失电子相等配平方程式;
解答:解:(1)实验室用氯化铵和氢氧化钙加热制取氨气,该反应是复分解反应,
故答案为:2NH
4Cl+Ca(OH)
2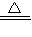
CaCl
2+2NH
3↑+2H
2O
(2)浓硝酸具有强氧化性,能和非金属单质C在加热条件下反应生成二氧化碳、二氧化氮和水,
故答案为:C+4HNO
3(浓)
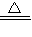
CO
2↑+4NO
2↑+2H
2O)
(3)反应方程式中元素的化合价变化为 FeCl
2→FeCl
3,铁元素由+2价→+3价,一个分子失去一个电子;
KNO
3→NO,氮元素由+5价→+2价,一个分子得3个电子,所以其最小公倍数为3,所以氯化亚铁的计量数为3,硝酸钾的计量数为1,其它元素根据原子守恒配平,所以该方程式为:
3 FeCl
2+1KNO
3+4 HCl=3FeCl
3+1KCl+1NO↑+2H
2O,
故答案为:3;1;4;3;1;1;2;
(4)反应方程式中元素的化合价变化为 SO
32-→SO
42-,硫元素由+4价→+6价,一个离子失去2个电子; MnO
4-→Mn
2+,
锰元素由+7价→+2价,一个离子得5个电子,所以其最小公倍数为10,故亚硫酸根离子的计量数为5,高锰酸根离子的计量数为2,其它元素根据原子守恒配平,所以该方程式为:5SO
32-+2 MnO
4-+6H
+=2Mn
2++5SO
42-+3H
2O.
故答案为:5;2;6;2;5;3;
点评:氨气的三种实验室制法:
1、加热固态铵盐和间的混合物;
2、加热浓氨水;
3、浓氨水中加固态碱性物质;

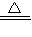 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O CO2↑+4NO2↑+2H2O)
CO2↑+4NO2↑+2H2O)

 阅读快车系列答案
阅读快车系列答案
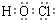
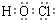
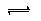 H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大 H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大




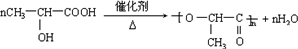

 +14CD2T2,在同样条件下,完成下列反应:2CH3CH2OD+C18O2
+14CD2T2,在同样条件下,完成下列反应:2CH3CH2OD+C18O2